الحالة الصلبة Solid’s State
الحالة الصلبة هي احدى حالات المادة الفيزيائية الثلاث.
تمتاز الحالة الصلبة بعدة خصائص منها:
* تترتب في أماكن محددة لا تغادرها وتتحرك في أماكنها حركة اهتزازية؛ وذلك لأنها متقاربة جدًا وأن قوى التجاذب بينها كبيرة.
* ذات شكل وحجم ثابتين؛ لأن كثافتها عالية، وغير قابلة للانضغاط أو الجريان.
عند تسخين المادة الصلبة تهتز جسيماتها بشكل أسرع مما يؤدي الى زيادة الطاقة الحركية للجسيمات، وبزيادة الطاقة الحركية تضعف قوى التجاذب بينها فتتحول من الحالة الصلبة الى الحالة السائلة عند درجة حرارة معينة تسمى درجة الانصهار.
تقسم المواد الصلبة الى نوعين رئيسين؛ مواد صلبة بلورية ومواد صلبة غير بلورية
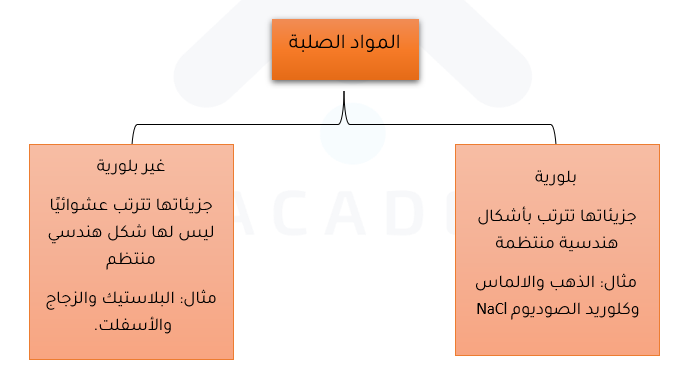
أتحقق صفحة 40: ما الفرق بين المواد الصُّلبة البلورية وغير البلورية؟
الحل: المواد الصُّلبة البلورية تترتب جسيماتها بحيث تكوّن أشكالًا هندسية منتظمة، أما غير البلورية فتترتب جسيماتها عشوائيًا أي ليس لها شكل هندسي منتظم.
المواد الصلبة البلورية Crystalline Solids
تتكون المادة الصلبة البلورية من جسيمات ( ذرات أو جزيئات أو أيونات ) وتترتب هذه الجسيمات بشكل هندسي منتظم .
تصنف المواد الصُّلبة البلورية بناءً على نوع الروابط أو قوى التجاذب بين جسيماتها الى أربعة أنواع:
1- المواد الصُّلبة الجزيئية Molecular Solids
تتكون من ذرات أو جزيئات تترابط مع بعضها بقوى تجاذب ضعيفة نسبيًا.
خصائص المواد الصُّلبة الجزيئية:
* تترابط جسيماتها بروابط هيدروجينية أو ثنائية القطب أو لندن.
* مواد هشة ذات درجات انصهار منخفضة.
* غير موصلة للتيار الكهربائي؛ لان جسيماتها متعادلة الشحنة ترتبط مع بعضها بقوى تجاذب ضعيفة.
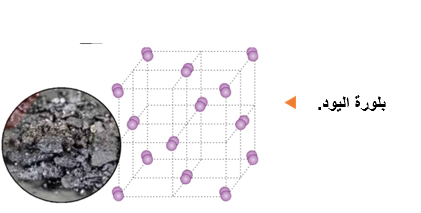
مثلًا: بلورة اليود تتكون من جزيئات اليود I2 المتعادلة التي تترابط بقوى لندن الضعيفة؛ لذلك درجة انصهاره منخفضة، كما ان بلوراته هشة وغير موصلة للتيار الكهربائي.
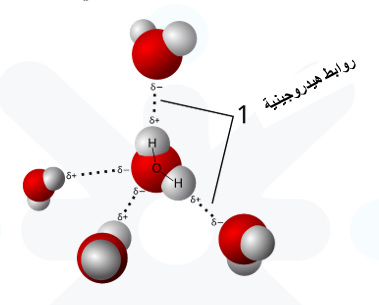
الجليد ايضًا، تترابط جزيئاته بروابط هيدروجينية، كل جزيء H2O يرتبط بأربعة جزيئات أخرى.
يكوّن الكربون مادة تسمى بكمنسترفولرين أو كرات باكي، تتكون من جزيئات كروية الشكل، ترتبط كل ذرة كربون في الجزيء الواحد بثلاث ذرات كربون أخرى بروابط تساهمية مكونة حلقات خماسية وسداسية مرتبطة مع بعضها البعض.
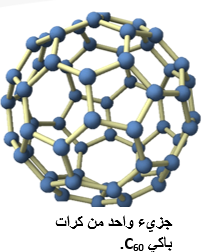
تترابط الكرات مع بعضها بقوى لندن الضعيفة، مكونة بلورات ابرية الشكل سوداء اللون تُسمى بكمنسترفولرين، وتمتاز هذه البلورات بأنها غير موصلة للتيار الكهربائي؛ لأنها تتكون من جزيئات متعادلة.
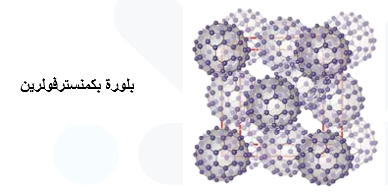
أتحقق صفحة 41: ما نوع الروابط بين ذرات الكربون داخل الجزيء الواحد من بكمنسترفولرين؟ وما نوع قوى التجاذب بين جزيئاته؟
الحل: نوع الروابط بين ذرات الكربون داخل الجزيء الواحد : تساهمية.
نوع قوى التجاذب بين جزيئاته: قوى لندن.
2- المواد الصُّلبة الشبكية التساهمية Covalent Network Solids
تتكون جسيماتها من ذرات تترابط فيما بينها بروابط تساهمية في بناء شبكي صلب، مثل الألماس والغرافيت والكوارتز SiO2 .
خصائص المواد الصُّلبة الشبكية التساهمية:
* تمتاز بالقساوة عدا الغرافيت.
* درجة الانصهار مرتفعة؛ وذلك لقوة الروابط التساهمية التي تربط بين ذراتها.
* غير موصلة للتيار الكهربائي في الحالتين الصلبة والسائلة – لان الكتروناتها مقيدة غير حرة الحركة- باستثناء الغرافيت.
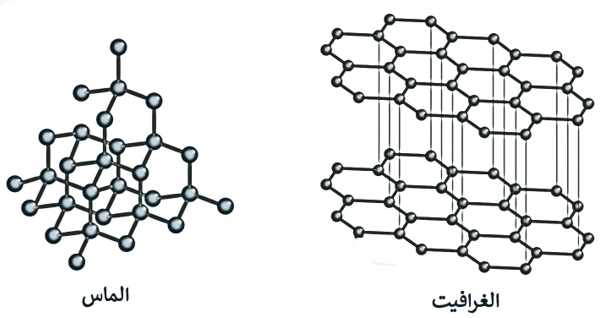
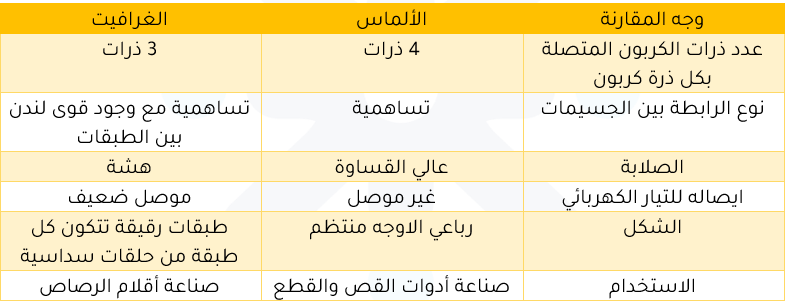
وفيما يلي جدول لأوجه التشابه والاختلاف بين الألماس والغرافيت
ظاهرة التآصل Allotropy
وهي ظاهرة وجود أكثر من شكل بلوري للعنصر الواحد في الحالة الفيزيائية نفسها.
يعتبر الالماس والغرافيت وبكمنسترفولرين متآصلات لان جميعها جسيماتها تتألف من ذرات الكربون.
أتحقق صفحة 42: أفسر: الغرافيت موصل جيد للكهرباء.
الحل: بسبب وجود روابط باي π بين ذرات الكربون؛ فإن الالكترونات المشاركة فيها تشكل ما يشبه السحابة بين الطبقات.
3- المواد الصلبة الفلزية Metallic Solids
تتكون جسيماتها من ذرات فلزات ترتبط برابطة فلزية فيما بينها.
خصائص المواد الصلبة الفلزية:
* درجات انصهارها مرتفعة على نحو عام؛ وذلك بسبب قوة الرابطة الفلزية.
* موصلة للتيار الكهربائي؛ ويعود ذلك لبحر الالكترونات السالبة حُرة الحركة في البلورة.
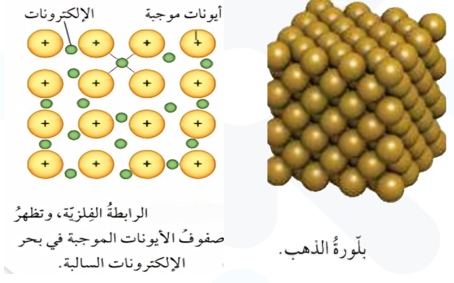
* قابلة للطرق والسحب؛ لان الطرق على صفوف الايونات الموجبة يجعلها تنزلق مبتعدة عن بعضها ولكنها تبقى مترابطة بفعل تجاذبها مع الالكترونات الحرة.
مثال: الصوديوم Na والمغنيسيوم Mg والنحاس Cu
أتحقق صفحة 43: أفسر قابلية المواد الصُّلبة الفلزية للطرق والسحب.
الحل: لأن الطرق على صفوف الايونات الموجبة يجعلها تنزلق مبتعده عن بعضها، ولكنها تبقى مترابطة بفعل تجاذبها مع الإلكترونات الحُرة.
 4- المواد الصلبة الأيونية Ionic Solids
4- المواد الصلبة الأيونية Ionic Solids
تتكون جسيماتها من أيونات موجبة وسالبة تتجاذب وتترابط برابطة أيونية.
مثال : كلوريد البوتاسيوم KCl وأكسيد الكالسيوم CaO
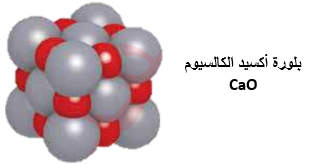
خصائص المواد الصُّلبة الأيونية
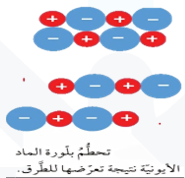
* شديدة الصلابة؛ وذلك بسبب الرابطة الأيونية القوية بين جسيماتها، رغم شدة صلابتها الا أنها هشة حيث انها اذا تعرضت للطرق فإن ايوناتها تنزلق ( تتحرك ) فتتقارب الايونات المتشابهه في الشحنة فتتنافر ، وهو ما يؤدي الى تحطم البلورة
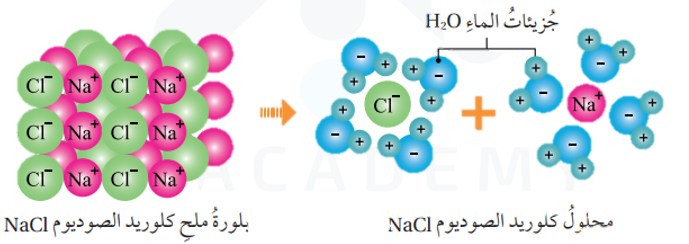
* غير موصلة للتيار الكهربائي في الحالة الصلبة؛ لان ايوناتها مقيدة- غير حرة الحركة- ولكن عند صهرها أو اذابتها في الماء تتحرر الايونات فتصبح موصلة للتيار الكهربائي.
* درجة انصهارها مرتفعة؛ بسبب قوة الرابطة الايونية بين جسيماتها.
أتحقق صفحة 44: أفسر: رغم صلابة المركبات الأيونية إلا أنها هشة.
الحل: لانه عند تعرضها للطرق؛ فإن ايوناتها تتحرك بالنسبة الى بعضها البعض، فتتقارب الايونات المتشابهة في الشحنة فتتنافر، وهو ما يؤدي الى تحطّم البلورة.
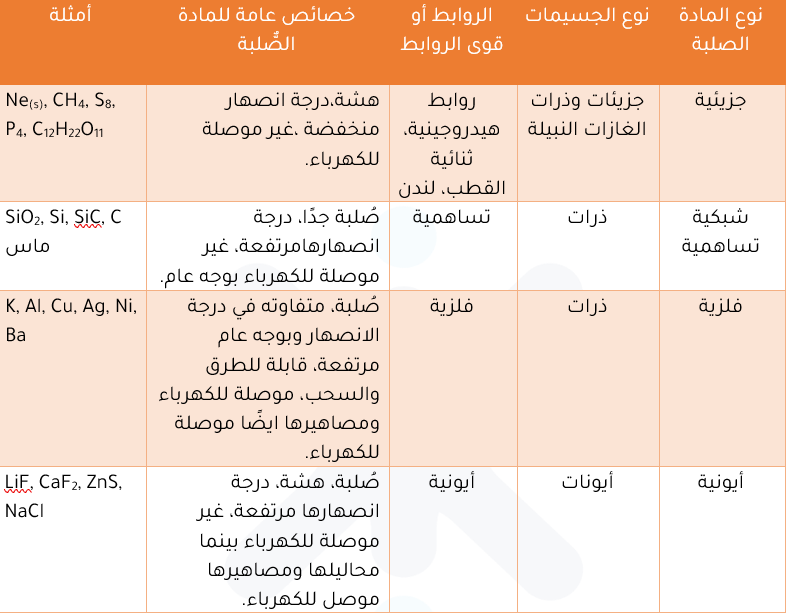
يوضح الجدول انواع المواد الصُّلبة البلورية والخصائص العامة لكل نوع.
مثال 1 :
أحدد نوع المادة الصُّلبة البلورية لكل مما يأتي :
أ. مادة( A ) بيضاء اللون تنصهر على درجة حرارة 730 C° غير موصلة للتيار الكهربائي، بينما محلولها موصل للكهرباء.
الحل: درجة انصهار المادة مرتفعة تشترك المواد الفلزية والايونية في هذه الصفة، وكذلك المادة A غير موصلة للكهرباء في الحالة الصلبة ولكن محلولها موصل وهذه الصفة مميزة للمركبات الأيونية، اذًا المادة A أيونية.
ب. مادة ( B ) شديدة الصلابة وشفافة وتنصهر عند درجة حرارة 3000 C° .
الحل: المادة شديدة الصلابة ودرجة انصهارها مرتفعة وهذه الصفات صفات المواد الشبكية التساهمية، اذًا المادة B شبكية تساهمية.
ج. مادة ( C ) صلبة ذات بريق معدني، موصلة جيدة للكهرباء ، قابلة للسحب والطرق، ذراتها مرتبة في شبكة بلورية.
الحل: المادة صُلبة وموصلة للكهرباء وقابلة للسحب والطرق هذه جميعها صفات المواد الفلزية، اذًا المادة C فلزية.
د. مادة ( D ) هشة ، لا توصل التيار الكهربائي، درجة انصهارها منخفضة.
الحل: المادة هشة وغير موصلة للتيار الكهربائي ، تشترك المواد الجزيئية والايونية في هذه الصفات، وكذلك المادة D درجة انصهارها منخفضة وهذه الصفة مميزه للمركبات الجزيئية.
مثال2: احدد نوع كل من المواد الصُّلبة الاتية: HF(s), Fe, Na2O, Si
الحل:
HF: جزيئية؛ لانها جزيئات ترتبط فيما بينها بروابط هيدروجينية.
Fe: فلزية؛ الحديد عبارة عن فلز وترتبط ذراته فيما بينها بروابط فلزية.
Na2O: أيونية؛ لانها تتكون من أيونات موجبة وسالبة والرابطة بين ايونات Na+ وايونات O2- رابطة أيونية.
Si: شبكية تساهمية؛ لأن ذرات Si تترابط بروابط تساهمية في بناء شبكي صُلب.