- المركبات الهيدروكربونية غير المشبعة :
المركبات الهيدروكربونية غير المشبعة هي مركبات تحتوي على الكربون والهيدروجين وتتميز بوجود روابط مزدوجة أو ثلاثية بين ذرات الكربون. وهذه المركبات تُعرف بالـ "ألكينات" (ذات الروابط المزدوجة) و"الألكاينات" (ذات الروابط الثلاثية).
على سبيل المثال:
- الألكينات: مثل الإيثيلين C2H4 الذي يحتوي على رابطتين مزدوجتين بين ذرتي كربون.
- الألكاينات: مثل الإيثاين C2H2 الذي يحتوي على رابطة ثلاثية بين ذرتي كربون.
المركبات غير المشبعة تفاعلية أكثر من المركبات المشبعة (مثل الألكانات) لأنها تحتوي على روابط غير مشبعة يمكن أن تتفاعل بسهولة مع مواد أخرى مثل الهالوجينات أو الأحماض.
- الألكينات:
الألكينات: هيدروكربونات غير مشبعة وتحتوي على رابطة تساهمية ثنائية بين ذرتي كربون متجاورتين، إحداهما قوية من نوع سيجما، والأخرى ضعيفة من نوع باي.
تحمل الألكينات الصيغة الجزيئية العامة:
حيث n رقم يبدأ من (2).
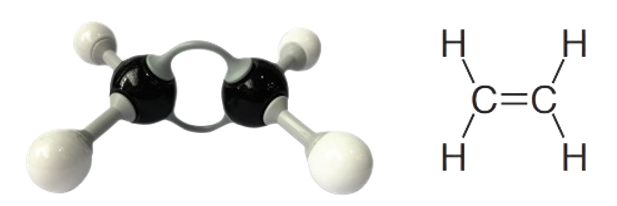
أبسط أنواع الألكينات الإيثين والذي يُعرف باسمه الشائع (الإيثيلين) ويحتوي على ذرتي كربون ويمتلك الصيغة الجزيئية C2H4، وكل ذرة كربون تعد مركز للمثلث المسطح، وتحصر الروابط فيما بينها زوايا مقدارها 120° ، ويكون تهجين ذرة الكربون المرتبطة بالرابطة الثنائية من نوع sp2، أما صيغته البنائية المختصرة فهي: CH2=CH2 .
- قواعد التسمية النظامية للألكينات:
1. اختر أطول سلسلة كربونية متتابعة تحتوي على الرابطة الثنائية.
2. رقّم السلسلة من الطرف الأقرب للرابطة الثنائية.
3. تسمية السلسلة الأطول باسم الألكان المقابل، مع استبدال المقطع (ين) بالمقطع (ان) بحيث يسبق الاسم رقم ذرّة الكربون الأقلّ في الرابطة الثنائية.
4. ترقيم مجموعات الألكيل المتفرّعة، وتسميتها بطريقة الألكانات نفسِها.
5. كتابة السم المركب كاملأً .
- مثال :
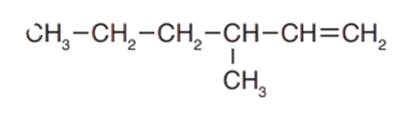
أُسمّي الألكين المجاور.
الحلُّ:
1 - أحدّد أطول سلسلة مستمرة من ذرّات الكربون تحتوي على الرابطة الثنائية.
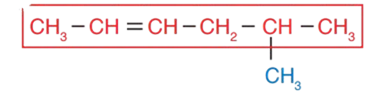
2 - أُرقّم هذه السلسلة من الطرف الأقرب إلى الرابطة الثنائية.
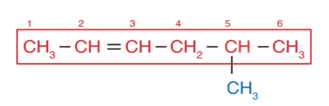
3-أُسمّي السلسلة الأطول باسم الألكان المقابلِ، مع استبدال المقطع (ين) بالمقطع (ان)،بحيث يسبق الاسم رقم ذرّة الكربون الأقلّ في الرابطة الثنائية فيُصبح الاسم 2- هكسين.
4- أُرقّم مجموعات الألكيل المتفرّعة، وأُسمّيها بالطريقة نفسها لتسمية الألكانات؛ وذلك بوضع اسم التفرّعات وأرقامها قبل اسم الألكين. في هذا المثال توجد مجموعة ميثيل تقع على ذرة الكربون فيصبح الاسم : 5- ميثيل .
5- اكتب اسم المركب كاملاً ، فيصبح اسم المركب النهائي : 5- ميثيل-2- هكسين.
- مثال :
أُسمّي الألكين المجاور.
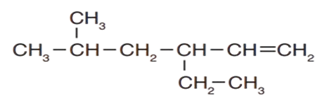
الحل:
1 - أحدّد أطول سلسلة مستمرّة من ذرّات الكربون تحتوي على الرابطة الثنائية:
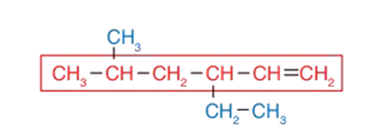
2- أُرقّم هذه السلسلة من الطرف الأقرب للرابطة الثنائية:
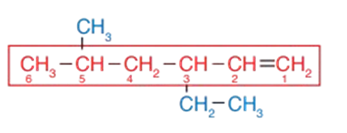
3 - أُسمّي السلسلة الأكثر طولا باسم الألكان المقابل مع استبدال المقطع (ين) بالمقطع (ان)، بحيث يسبق الاسم رقم ذرّة الكربون الأقلّ في الرابطة الثنائية فيصبح 1- هكسين.
4- أُرقّم مجموعات الألكيل المتفرّعة، وأُسمّيها بالطريقة نفسها لتسمية الألكانات؛ وذلك بوضع اسم التفرّعات وأرقامها قبل اسم الألكين. في هذا المثال نبدأُ بالإيثيل؛ لأنها تسبق أبجديًّا حسب اللغة الإنجليزية، ومن ثم الميثيل، فتصبح: 3- إيثيل – 5- ميثيل .
5- أکتبُ اسم المُركب كاملا ؛ فيصبح اسم الإلكين : 3- إيثيل -5- ميثيل – 1- هكسين.
- مثال:
ارسم الصيغة البنائية للمركب 3- ميثيل – 1- هكسين .
الحل :
1 - أرسم السلسلة المستمرّة التي تُمثّل الهكسين المحتوي على 6 ذرّات كربون، وأُرقّمها بحيث تكون الرابطة الثنائية على ذرّة الكربون رقم (1).
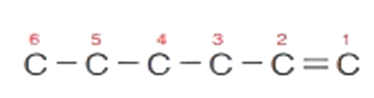
2 - أضع مجموعة الميثيل على ذرّة الكربون رقم (3).
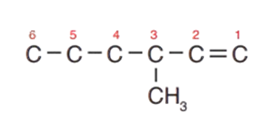
3 - أضيفُ ذرّات الهيدروجين على ذرّات الكربون، بحيث تُكوّن كلّ ذرّة كربون 4 روابط؛ فيصبح الشكل النهائي:
بعض الألكينات وخصائصها الفيزيائية.

الخصائص الفيزيائية والكيميائية للألكينات:
- الخصائص الفيزيائية:
تتشابه الألكينات في خصائصها الفيزيائية مع الألكانات.
الذائبية في الماء :
لا تذوب الألكينات في الماء؛ لكونها مركبات غير قطبية.
درجات الغليان :
درجات غليان الألكينات منخفضة؛ لوجود قوى لندن الضعيفة بين جزيئاتها، وتزداد درجات غليان الألكين بزيادة عدد ذرات الكربون فيه (الكتلة المولية).
الحالة الفيزيائية :
الألكينات الثلاثة الأولى غازية، ثم تصبح سائلة إلى الألكين الذي يحتوي على 15 ذرة كربون، ثم تصبح صلبة؛ والسبب في ذلك يعود لزيادة قوى لندن بزيادة عدد ذرات الكربون (الكتلة المولية) فتتحول الألكينات من الحالة الغازية إلى السائلة ومن ثم الصلبة.
- الخصائص الكيميائية :
الألكينات أنشط من الألكانات ، لاحتواء الرابطة الثنائية فيها على رابطة ضعيفة من نوع باي التي يسهل كسرها اثناء التفاعل .
الاحتراق:
يحترق الألكين بوجود الأكسجين، وينتج من احتراقه غاز ثاني أكسيد الكربون وبخار الماء وكمية من الطاقة.
مثال:
تفاعل احتراق الإيثين C2H4 :
- أكسدة الألكينات:
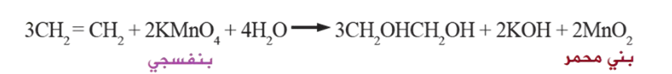
تتأكسد الألكينات باستخدام محلول بيرمنغنات البوتاسيوم KMnO4 البارد ذي اللون البنفسجي، فتكسر الرابطة الثنائية وينتج مركب عضوي يحتوي على مجموعتي هيدروكسيل (OH)، ويتكون راسب بني محمر من أكسيد المنفنيز MnO2 .
- تفاعلات الإضافة:
تحدث تفاعلات الإضافة في الألكين على الرابطة الثنائية، فتنكسر رابطة باي وتتكون رابطتي سيجما على ذرتي كربون الرابطة الثنائية، وينتج مركب مشبع.
من أمثلة تفاعلات الإضافة في الألكينات تفاعل إضافة الهيدروجين إلى الألكين بوجود النيكل أو البلاتين كعامل مساعد ويتكون الألكان المقابل.
مثال: إضافة الهيدروجين إلى الإيثين لتكوين الإيثان:
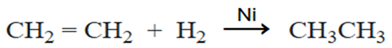
- الألكاينات:
الألكاينات: هيدروكربونات غير مشبعة وتحتوي على رابطة مشتركة ثلاثية بين ذرتي كربون متجاورتين .
تحمل الألكاينات الصيغة الجزيئية العامة:
حيث n رقم يبدأ من (2).
أبسط أنواع الألكاينات جزيء الإيثاين والذي يعرف باسمه الشائع (الأسيتيلين) ويحتوي على ذرتي كربون بينهما رابطة ثلاثية (رابطة من نوع سيغما، ورابطتان من نوع باي)، ويمتلك الصيغة الجزيئية C2H2 ، وهو جزيء خطي وتبلغ قيمة الزاوية . بين روابطه 180°، ويكون تهجين الكربون فيه من نوع sp.

- تسمية الألكاينات:
تُسمّى الألكاينات بالطريقة نفسها لتسمية الألكينات، ويُشتقُّ اسمها من الألكانات المقابلة باستبدال المقطع (اين) بالمقطع (ان) في سلسلة الألكان المقابلة وفق الخطوات الآتية:
1- تحديد السلسلة المستمرة الأكثر طولًا التي تحتوي على الرابطة الثلاثية.
2- ترقيم السلسلة من الطرف الأقرب إلى الرابطة الثلاثية.
3- تسمية السلسلة الأكثر طولًا باسم الألكان المقابل مع استبدال المقطع (اين) بالمقطع (ان)، بحيث يسبق الاسم رقم ذرّة الكربون الأقلّ في الرابطة الثلاثية.
4- ترقيم مجموعات الألكيل المتفرّعة، وتسميتها بالطريقة نفسها لتسمية الألكانات .
5- كتابة اسم المركب كاملاً .
- مثال :
أُسمّي المُركّب المجاور.
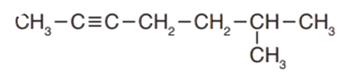
الحلُّ:
1 - أحدّد السلسلة المستمرة الأطول التي تحتوي على الرابطة الثلاثية.
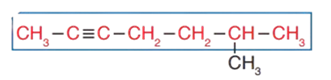
2- أُرقّم هذه السلسلة من الطرف الأقرب إلى الرابطة الثلاثية كما في الشكل:
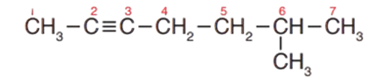
3 - أُسمّي السلسلة الأطول باسم الألكان المقابل مع استبدال المقطع (اين) بالمقطع (ان)، بحيث يسبق الاسم رقم ذرّة الكربون الأقلّ في الرابطة الثلاثية؛ فيصبح اسم الألكاين: هبتاين.
4 - أُرقّم مجموعات الألكيل المتفرّعة، وأُسمّيها بالطريقة نفسها لتسمية الألكانات، وألاحظ وجود مجموعة ميثيل تقع على ذرّة الكربون السادسة؛ فيصبح اسمها: 6- ميثيل.
5- أكتب المركب كاملا فيصبح : 6- ميثيل -2- هباتين
مثال :
أرسم الصيغة البنائية للألكاين -4- إيثيل -1- هكساين ؟
الحل:
1 - أرسم 6 ذرّات كربون تُمثّل الهكساين، وأضع الرابطة الثلاثية على الذرّة الأولى.
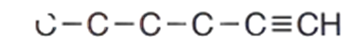
2 - أُرقّم السلسلة من الطرف الأقرب إلى الرابطة الثلاثية.
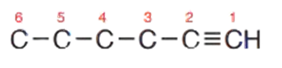
3- أضع مجموعة الإيثيل -CH,CH2 على ذرّة الكربون رقم 4؛ فيصبح الشكل البنائي:
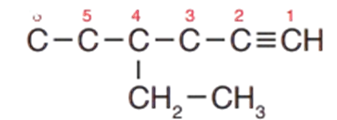
4- أضع ذرّات الهيدروجين على السلسلة؛ بحيث تصبح كلّ ذرّة كربون مرتبطة بأربع روابط كما في الشكل المجاور:
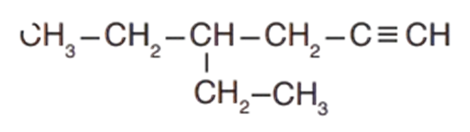
الخصائص الفيزيائية والكيميائية للألكاينات :
الخصائص الفيزيائية :
تتشابه الألكاينات في خصائصها الفيزيائية مع الإلكينات والألكانات.
الذائبية في الماء :
لا تذوب الألكاينات في الماء؛ لكونها مركبات غير قطبية.
درجات الغليان:
درجات غليان الألكاينات منخفضة؛ لوجود قوى لندن الضعيفة بين جزيئاتها، وتزداد
درجات غليان الألكين بزيادة عدد ذرات الكربون فيه (الكتلة المولية).
الحالة الفيزيائية
الألكاينات الثلاثة الأولى غازية، ثم تصبح سائلة ثم صلبة بزيادة ثم تصبح صلبة عدد
ذرات الكربون (الكتلة المولية)؛ والسبب في ذلك يعود لزيادة قوى لندن.
- الخصائص الكيميائية :
الألكاينات أنشط من الألكانات، لاحتواء الرابطة الثلاثية فيها على رابطتين ضعيفتين من نوع باي التي يسهل كسرها أثناء التفاعل.
الاحتراق :
يحترق الألكاين بوجود الأكسجين، وينتج من احتراقه غاز ثاني أكسيد الكربون وبخار الماء وكمية من الطاقة.
مثال: تفاعل احتراق الإيثاين (الأسيتلين) C2H2:
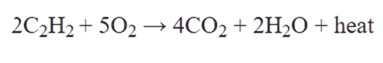
تفاعلات الإضافة :
تحدث تفاعلات الإضافة في الألكاين على الرابطة الثلاثية، فتنكسر رابطتي باي وتتكون (4) روابط من نوع سيجما على ذرتي كربون الرابطة الثلاثية.
الإثراء والتوسّع :
هرمون الإيثين
Ethene Hormone
الهرمونات النباتية مُركّبات عضوية تُنتِجُها النباتات بكميات قليلة، وتُسرّع نموّ النبات، ومن هذه الهرمونات: هرمون الإيثين، واسمه الشائع (هرمون الإيثلين)؛ وهو هرمون نباتيّ طبيعيّ يوجد في الحالة الغازية، بعكس الهرمونات النباتية الأخرى، ويُصنَّع في الثمار، وله دور في نُضجها، ويُستخدَم في إنضاج الثمار داخل الغرف المُخصّصة لتخزينِها، فحين تُقطَف الفواكه قبل نضجها لإتاحة الوقت لنقلها تُعرَّض ثمارها إلى مصدر يبعث غاز الإيثين حال وصولها الغرف المُخصّصة للتخزين، ما يعجّل نُضجها لتُعرَض على المستهلك، كما في عملية إنضاج ثمار الموز، والمانغا، والبندورة، وغيرها. كما أنه يُسبّب تلفَ الفواكه عند زيادة كمية استخدامه. المشكلة تبدأ حين يلفُّ غاز الإيثين محيط فاكهة لم تنضج بعد، فوجوده يشجّع تلك الفاكهة على النضج السريع فتسبق أوانها، وحين تكون ناضجةً يُحفّزها على مزيد من النضج، ومن ثَم ستتعفّن وتصبح غير صالحة للأكل، ويمكن ملاحظة هذه الظاهرة عند وضع مجموعة مختلفةِ الأنواع من الفواكه، ومنها التفاح، في طبق واحد، إذ يلاحَظ تعفَّن هذه الثمار بصورة أسرع؛ بسبب إطلاق التفاح غاز الإيثين أكثر من غيره من الفواكه الأخرى؛ لذا يُعزَل التفاح عن هذه الفواكه، ويجب ألّا تقلّ المسافة بين الأطباق عن نصف متر في أقلّ تقدير، ولا يقتصر هذا على التفاح؛ بل يشمل البندورة، والمشمش، والإجاص، والخوخ، وجميعُها من بواعث غاز الإيثين.
