امتحان تجريبي كيمياء
امتحان تجريبي كيمياء
عدد الاسئلة : 50 أسئلة
امتحان تجريبي كيمياء
00 : 00 دقيقة
1- المادة التي تسلك سلوكاً حمضياً وفق مفهوم كل من أرهينيوس وبرونستد-لوري ولويس:
2- أحد الآتية زوج مترافق ينتج من تفاعل HCOO- مع ،هو:
3- العبارة الصحيحة في المعادلة: هي:
5- عند خلط حجوم متساوية من محلول LiOH (pH = 11) مع محلول HI مجهول التركيز، كانت pH للمحلول الناتج = 7، فإن تركيز HI قبل الخلط يساوي:
6- في محلول ما، إذا كانت
8- إذا علمت أن pH لمحلول الحمض HNO2 تساوي قيمة pH لمحلول الحمض HBr عندما يكون تركيز HBr = (7 × 10-3 M) ، فإن تركيز الحمض HNO2(M)، يساوي: (Ka HNO2 = 4.9 × 10-4)
9- محلول من القاعدة الضعيفة B تركيزه (0.1 M) فإن pH للمحلول:
10- ادرس المعلومات الآتية للقواعد الافتراضية (A, B, C) المتساوية في التركيز،
- تركيز [OH-] في محلول A أعلى منه في محلول B.
- قيمة Kb للقاعدة B أقل من قيمة Kb للقاعدة C.
- محلول الملح CHCl أكثر قدرة على التميّه من محلول الملح AHCl عند التركيز نفسه.
تُؤدي إضافة بلورات الملح CHCl إلى محلول القاعدة C إلى:
11- محلول منظم يتألف من الحمض الضعيف HCOOH والملح HCOONa، وعند إضافة (0.1 M) HBr أصبح تركيز الحمض والملح يساوي (0.4 M) و(0.8 M) على الترتيب.
(log 9 = 0.95 // Ka: HCOOH = 1.8 × 10-4 )
قيمة pH للمحلول المنظم بعد إضافة HBr إليه، تساوي: (أهمل التغيّر في الحجم)
** يبين الجدول التالي معلومات لعدد من محاليل حموض ضعيفة ومحاليل الأملاح، تركيز كل منها (0.01 M)،
أدرسه ثم أجب عن الأسئلة (12 → 13)
pH * لمحلول الملح NaX أعلى من pH لمحلول الملح NaQ
[H3O+] * في محلول الملح NaY أقل من تركيز [H3O+] في محلول الملح NaQ
pOH * لمحلول HX وملحه NaX = 9.8
[Q-] * في محلول الحمض HQ أقل من تركيز [Z-] في محلول الحمض HZ
*تركيز Y- في محلول الحمض HY = 2.6 × 10-3 M
12- أعلى تركيز
** يبين الجدول التالي معلومات لعدد من محاليل حموض ضعيفة ومحاليل الأملاح، تركيز كل منها (0.01 M)،
أدرسه ثم أجب عن الأسئلة (12 → 13)
pH * لمحلول الملح NaX أعلى من pH لمحلول الملح NaQ
[H3O+] * في محلول الملح NaY أقل من تركيز [H3O+] في محلول الملح NaQ
pOH * لمحلول HX وملحه NaX = 9.8
[Q-] * في محلول الحمض HQ أقل من تركيز [Z-] في محلول الحمض HZ
*تركيز Y-في محلول الحمض HY = 2.6 × 10-3 M
13- الملح الأقل قدرة على التميّه، هو:
14- نصف التفاعل الذي يزداد عدد تأكسد النيتروجين (N) فيه بمقدار (4)، هو:
15- عدد مولات أيونات الهيدروكسيد - OHاللازم إضافتها إلى طرفي المعادلة لموازنة التفاعل الآتي في وسط قاعدي: هو
16- أحد التفاعلات غير الموزونة الآتية يُمثل تفاعل تأكسد واختزال ذاتي:
17- عند خلط محلول KMnO4مع محلول HCl، تكوّنت فقاعات من غاز CI2 ، وتواجدت أيونات Mn+2 في المحلول، أي من التغيرات الآتية حدثت:
18- خلية جلفانية أعطيت الرمز الآتي: Cr|Cr+3||Ag+|Ag ، فإن العبارة الصحيحة هي:
** يتضمن الجدول المجاور عدداً من الخلايا الجلفانية لعناصر فلزية لها رموز افتراضية، لأيوناتها شحنة ثنائية موجبة في مركباتها، ومعلومات عنها. ادرسه ثم أجب عن الفقرات (19 – 22). علماً بأن قيمة Eo لنصف تفاعل الاختزال الآتي يساوي (-2.37V)
19- صيغة الأيون الذي يستطيع أكسدة الفلز G ولا يستطيع أكسدة الفلز M:
** يتضمن الجدول المجاور عدداً من الخلايا الجلفانية لعناصر فلزية لها رموز افتراضية، لأيوناتها شحنة ثنائية موجبة في مركباتها، ومعلومات عنها. ادرسه ثم أجب عن الفقرات (19 – 22). علماً بأن قيمة Eo لنصف تفاعل الاختزال الآتي يساوي (-2.37V)
20- العامل المختزل الأضعف هو:
** يتضمن الجدول المجاور عدداً من الخلايا الجلفانية لعناصر فلزية لها رموز افتراضية، لأيوناتها شحنة ثنائية موجبة في مركباتها، ومعلومات عنها. ادرسه ثم أجب عن الفقرات (19 – 22). علماً بأن قيمة Eo لنصف تفاعل الاختزال الآتي يساوي (-2.37V)
 21- خلية جلفانية قطباها (X / M)، فإن جهدها المعياري
21- خلية جلفانية قطباها (X / M)، فإن جهدها المعياري
** يتضمن الجدول المجاور عدداً من الخلايا الجلفانية لعناصر فلزية لها رموز افتراضية، لأيوناتها شحنة ثنائية موجبة في مركباتها، ومعلومات عنها. ادرسه ثم أجب عن الفقرات (19 – 22). علماً بأن قيمة Eo لنصف تفاعل الاختزال الآتي يساوي (-2.37V)
 22- في الخلية الجلفانية قطباها (Z / Y)، فإن العبارة الصحيحة:
22- في الخلية الجلفانية قطباها (Z / Y)، فإن العبارة الصحيحة:
23- خلية جلفانية قطباها (X , Y)، الأيون
24- بالاعتماد على جدول جهود الاختزال المجاور؛ عند عمل تحليل كهربائي لمحاليل الأملاح (CuI2 , AgBr , ZnBr2) ، فإن ترتيب الذرات (الجزيئات) بالتكوّن عند المهبط، هو:

25- إذا علمت أن الشكل المجاور يُمثل خلية تحليل كهربائي لتنقية الفلزات من خاماتها..بالاطلاع على المعلومات الواردة على الشكل؛ ترتيب الذرات حسب جهود تأكسدها هو:
26- البيانات الواردة في الجدول المجاور تخص التفاعل التالي أدرس الجدول، ثم أجب
سرعة استهلاك N2O5 في الفترة الزمنية s(16, 24) بوحدة M/s: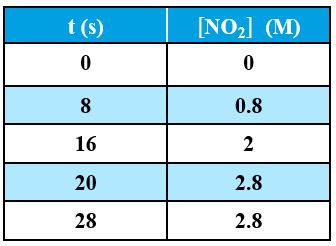
27- في التفاعل الافتراضي ، إذا كانت سرعة إنتاج (D) تساوي 3.3 × 10-7 M/s في الفترة الزمنية s(4800 – 5400)، فإن سرعة إنتاج (D) في الفترة الزمنية s(1200 – 1800) تُساوي: (M/s)
28- الرسم البياني المجاور يُمثل تركيز المادة الناتجة A مقابل الزمن، إذا علمت أن السرعة الابتدائية للتفاعل تساوي ثلاثة أضعاف السرعة اللحظية عند الزمن s(20)، فإن مقدار السرعة المتوسطة للتفاعل بوحدة (M.s-1) ، تساوي: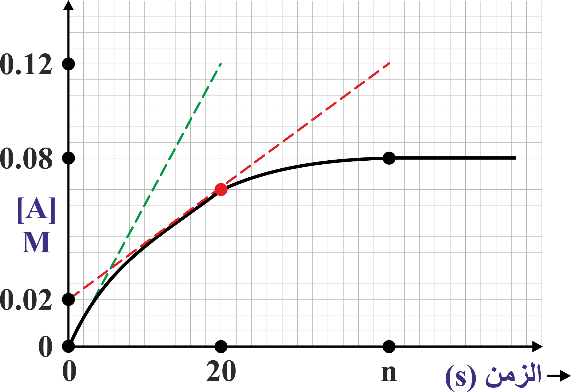
29- تم قياس تركيز مادة متفاعلة B بشكل دوري وتسجيله في الجدول الآتي:
فأن قانون سرعة التفاعل:
** للتفاعل: A + BC ، تم تسجيل البيانات الواردة في الجدول المجاور عند درجات حرارة مختلفة؛ أجب عن الفقرات (31 - 30):
30- وحدة ثابت السرعة k، هي:
** للتفاعل: A + BC ، تم تسجيل البيانات الواردة في الجدول المجاور عند درجات حرارة مختلفة؛ أجب عن الفقرات (31 - 30):
31- قيمة ثابت السرعة k، في تجربة (4):
32- التفاعل الأسرع فيما يأتي:
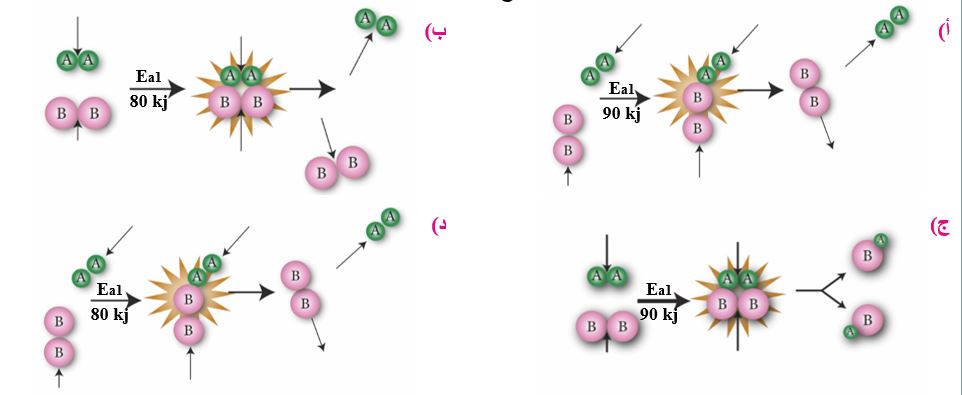
33- أي التصادمات الآتية يُعتبر اتجاه تصادم صحيح وطاقة غير كافية:
** للتفاعل A + X 2B حيث (X) تُمثل الطاقة المصاحبة للتفاعل بوحدة (kj)، إذا علمت أن:
* طاقة المواد الناتجة = 3X
* طاقة المواد المتفاعلة = (40 + X)
* طاقة التنشيط للتفاعل العكسي = (20 + X)
وعند إضافة عامل مساعد إلى وعاء التفاعل انخفضت طاقة التنشيط للتفاعل الأمامي بمقدار نصف قيمة X، أجب عن الفقرات (36 – 34)
34- الطاقة المصاحبة (X) بوحدة (kj)، تُساوي:
** للتفاعل A + X 2B حيث (X) تُمثل الطاقة المصاحبة للتفاعل بوحدة (kj)، إذا علمت أن:
* طاقة المواد الناتجة = 3X
* طاقة المواد المتفاعلة = (40 + X)
* طاقة التنشيط للتفاعل العكسي = (20 + X)
وعند إضافة عامل مساعد إلى وعاء التفاعل انخفضت طاقة التنشيط للتفاعل الأمامي بمقدار نصف قيمة X، أجب عن الفقرات (36 – 34)
35- طاقة المعقّد المنشَط بوجود عامل مساعد بوحدة (kj)، تُساوي:
** للتفاعل A + X 2B حيث (X) تُمثل الطاقة المصاحبة للتفاعل بوحدة (kj)، إذا علمت أن:
* طاقة المواد الناتجة = 3X
* طاقة المواد المتفاعلة = (40 + X)
* طاقة التنشيط للتفاعل العكسي = (20 + X)
وعند إضافة عامل مساعد إلى وعاء التفاعل انخفضت طاقة التنشيط للتفاعل الأمامي بمقدار نصف قيمة X، أجب عن الفقرات (36 – 34)
36- طاقة التنشيط للتفاعل الأمامي دون وجود عامل مساعد بوحدة (kj)، تُساوي:
37- المادة الكيميائية المُضافة بنسب مُحدّدة إلى الخلطة الإسمنتية (الخرسانة) لزيادة سرعة تصلبها في فصل الشتاء، هي:
38- في التفاعل الآتي:
39- أي الكحولات الآتية لا يتم تحضيره بواسطة مركب غرينارد:
40- يمكن تحضير الإيثر من احد التفاعلات الآتية هو:
41- يتفكك المركب HCOOCH2CH2CH2CH3عند تسخينه مع محلول قاعدة قوية منتجاً مركبين عضويين، عند تسخين أحدهما مع حمضH2SO4 المركز نتج المركب العضوي (A)؛ الذي يتفاعل مع الماء بوسط حمضي منتجاً المركب العضوي (B)؛ وهذا بدوره يتفاعل معH3PO4 المركز الساخن فينتج المركب العضوي (X)؛ والذي له الصيغة الآتية:
42- المركب الذي لا يُمكن تحضير برومو إيثان CH3CH2Br منه بخطوة واحدة، هو:
43- عند اختزال الكيتونات إلى كحولات ثانوية، يُستخدم NaBH4 في وسط من:
44- في التفاعل الآتي: فإن ذرة H التي تحمل إشارة النجمة *، مصدرها:
45- يُعد تفاعل البروبانونCH3COCH3 مع ميثيل كلوريد المغنيسيومCH3CgCI مثالاً على:
46- أي المركبات الآتية لا ينتج بالتكسير الحراري للألكانات:
47- الناتج العضوي في التفاعل الآتي، هو:
48- في التفاعل الآتي: ؛ فإن العامل المساعد A، هو:
49- في التفاعل الآتي: ؛ يعود السبب في تكوين CH3CH = CHCH3 وليس CH3CH2CH=CH2 بسبب:
50- عند تحضير
4- كتلة المُذابة في من الماء النقي لتتغير pH بمقدار ; تساوي:
7- إذا علمت أن , وكان لديك من محاليل هذه القواعد كميات متساوية في pH ومتساوية في حجومها؛ فأي العبارات الآتية غير صحيحة: