مراجعة الدرس الثالث
1- الفكرة الرئيسة: أوضح كيف تفسر نظرية التصادم حدوث التفاعل الكيميائي.
تفترض نظرية التصادم أنه يجب تصادم الجسيمات المتفاعلة بالاتجاه الصحيح وأن تمتلك الطاقة الكافية لتكسير الروابط بين الجسيمات المتفاعلة لتكوين روابط جديدة.
2- أوضح المقصود بكل من: المعقد المنشط، العامل المساعد
طاقة التنشيط: الحد الأدنى من الطاقة الحركية التي يجب أن تمتلكها الجسيمات المتفاعلة كي تبدأ التفاعل وتكون روابط جديدة.
العامل المساعد: مادة تزيد من سرعة التفاعل الكيميائي دون أن تستهلك أثناء التفاعل.
3- أفسر أثر كل مما يأتي في سرعة التفاعل الكيميائي:
تركيز المواد المتفاعلة، درجة الحرارة، مساحة سطح المواد المتفاعلة.
تركيز المواد المتفاعلة: بزيادة عدد الجسيمات المتفاعلة في وحدة الحجم يزداد عدد التصادمات الكلية بينها فتزداد فرصة تصادم الجسيمات بينها في الاتجاه الصحيح ( وبوجود الطاقة الكافية) فيزداد عدد التصادمات الفعالة وتزداد سرعة التفاعل.
مساحة سطح الجسيمات الفعالة: زيادة سطح المواد الصلبة المعرضة للتفاعل فيزداد عدد التصادمات الفعالة فتزداد سرعة التفاعل.
4- أستنتج من البيانات الواردة في الجدول الآتي:
| البيانات | طاقة المواد الناتجة | التغير في المحتوى الحراري | طاقة المعقد المنشط بوجود عامل مساعد | طاقة التنشيط للتفاعل العكسي دون عامل مساعد |
| تاطاقة kJ | 50 | 20+ | 70 | 110 |
أ- طاقة المواد المتفاعلة kJ 30
ب. طاقة التنشيط للتفاعل العكسي بوجود عامل مساعد kJ 20
ج. طاقة التنشيط للتفاعل الامامي دون عامل مساعد kJ 130
د. طاقة المعقد المنشط دون عامل مساعد kJ 160
هـ. ماص
و. طاقة تنشيط التفاعل الأمامي بوجود عامل مساعد kJ 40
5-إلامَ تشير الأرقام المبيّنة في الشكل الآتي:
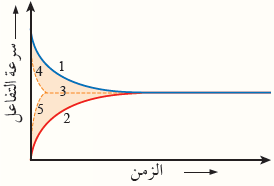
1-سرعة التفاعل الأمامي بدون عامل مساعد
2-سرعة التفاعل العكسي بدون عامل مساعد.
3-حالة الاتزان الكيميائي.
4-سرعة التفاعل الأمامي بوجود عامل مساعد.
5-سرعة التفاعل العكسي بوجود عامل مساعد.
6- أيّ من الآتية يؤثر فيها العامل المساعد: طاقة المواد المتفاعلة، طاقة تنشيط التفاعل العكسي، طاقة المعقّد
المنشّط، التغيّر في المحتوى الحراري للتفاعل، زمن حدوث التفاعل، موضع الاتزان.
طاقة تنشيط التفاعل العكسي / طاقة المعقد المنشط / زمن حدوث التفاعل
7- في التفاعل الافتراضي الآتي A + B → C + D + 80 kJ ، طاقة التنشيط للتفاعل الأمامي 55 kJ وطاقة الموادّ الناتجة 15 kJ ، أجد قيمة كلّ ممّا يأتي بوحدة kJ
أ. طاقة التنشيط للتفاعل العكسي.135
ب. طاقة المعقّد المنشّط.150
----------------------------------------------------------------------------------------
أسئلة الوحدة المتعلقة بالدرس الثالث:
1. أوضح المقصود ب: طاقة تنشيط التفاعل:الحد الأدنى من الطاقة الحركية التي يجب أن تمتلكها الجسيمات المتفاعلة كي تبدأ التفاعل وتكون روابط جديدة.
2. أفسّر ما يأتي:
أ لا تؤدي جميع التصادمات إلى حدوث تفاعل كيميائي.
ب زيادة سرعة التفاعل بإضافة عامل مساعد.
أ) لأنه قد لا يتوفر الاتجاه الصحيح( المناسب) والطاقة الكافية في الجسيمات المتصادمة.
ب)العامل المساعد يمهد مسار بديل أكثر سهولة مما يقلل طاقة التنشيط للتفاعل فتزداد سرعة التفاعل.
5. يمثل الشكلان ( أ ، ب) تفاعلًا في ظرفين مختلفين.
أستنتج أي الشكلين يمثل التفاعل الأسرع؟ وأحدد العامل المؤثر في سرعة هذا التفاعل؟

(ب) العامل المؤثر هو التركيز فيتضح من الشكل زيادة عدد الجسيمات في وحدة الحجم وبالتالي زيادة عدد التصادمات الفعالة.
8. أتوقع من الشكلين الآتيين ( أ، ب) الشرط الذي أدّى إلى حدوث التفاعل الكيميائي، ثم أفسّر إجابتي.
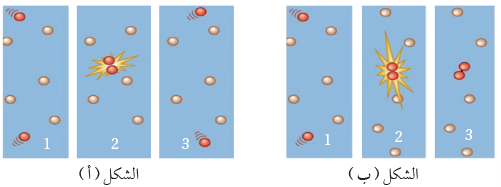
يلاحظ من الشكلين أ/2 و ب/2 أنه حدث تصادم بين جسيمين متفاعلين في الإتجاه الصحيح، ولكن في الشكل أ/3 ارتد الجسيمان عن بعضهما. أما في الشكل ب/3 فإن الجسيمان ارتبطا ببعضهما ما يدل على أنه حدث تصادم فعال وأن العامل المؤثر هو توفر الطاقة الكافية للتصادم.
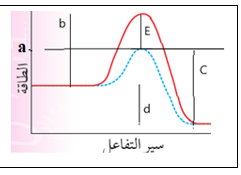
9. طاقة المعقد المنشط بوجود عامل مساعد a
طاقة تنشيط التفاعل الأمامي دون عامل مساعد b
طاقة تنشيط التفاعل العكسي بوجود عامل مساعد c
التغير في المحتوى الحراري d
الانخفاض في طاقة المعقد المنشط نتيجة اضافة عامل مساعد E
12.
2. العبارة الصحيحة في ما يتعلق بالعامل المساعد:
أ ) يزيد من طاقة التنشيط للتفاعل ب) يقلل من طاقة المعقّد المنشّط
ج) يقلل المحتوى الحراري للتفاعل د ) يزيد من طاقة النواتج
3. عند زيادة مساحة سطح المادة المتفاعلة المعرض للتفاعل عند الظروف نفسها؛ فإن العبارة الصحيحة:
أ ) تقلّ سرعة التفاعل ب) يزداد التركيز ج) تزداد عدد التصادمات الفعالة د ) تقلّ درجة الحرارة
4. إذا كانت طاقة التنشيط للتفاعل الامامي 70kJ وكان التغيّر في المحتوى الحراري 50kJ - ؛ فإن طاقة التنشيط
للتفاعل العكسي تساوي بوحدة :kJ
أ ) 20 ب) 50 ج) 70 د ) 120
5 . في تفاعل ما تؤدي زيادة درجة حرارة التفاعل إلى:
أ ) زيادة طاقة التنشيط ب) تقلّيل سرعة التفاعل
ج) زيادة عدد التصادمات الفعالة د ) تقلّيل متوسط الطاقة الحركية
7. في تفاعل ما كانت طاقة التنشيط للتفاعل الأمامي ( 70 kJ )، وطاقة التنشيط للتفاعل العكسي ( 50 kJ )؛ فإن قيمة
التغير في المحتوى الحراري للتفاعل تساوي :
أ ) + 20 ب) - 20 ج) + 120 د ) - 120
8 . تفاعل فلزّ المغنيسيوم مع الماء أبطأ من فلز الصوديوم في الظروف نفسها، ويعود ذلك إلى:
أ ) درجة الحرارة ب) طبيعة المتفاعلات ج) التركيز د ) العامل المساعد
13. يبين الشكل الآتي تغير الطاقة خلال سير التفاعل أدرس الشكل وأجيب عن الأسئلة الآتية:
ما القيمة لكلًّ مما يأتي:
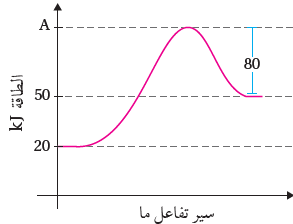
أ) طاقة المعقّد المنشّط. 130
ب ) التغيّر في المحتوى الحراري. +30
ج)طاقة تنشيط التفاعل الأمامي. 110
و )إذا أُضيف عامل مساعد كتلته 3g ، وانخفضت طاقة المعقد
المنشّط بمقدار 10kJ ، فما قيمة طاقة التنشيط للتفاعل
الأمامي بعد إضافة العامل المساعد؟100
ه) ما كتلة العامل المساعد بعد انتهاء التفاعل؟3g
14.
| سير التفاعل | طاقة المواد الناتجة | طاقة المعقد المنشط | طاقة تنشيط التفاعل العكسي | طاقة تنشيط التفاعل الأمامي |
| دون عامل مساعد | أ | ب | 170 | ج |
| بوجود عامل مساعد | 40 | 150 | د | 80 |
|
أ |
ب |
ج |
د |
|
40 |
210 |
110 |
140 |