مفهوم الحالة السائلة:
- إحدى حالات المادة الأربع.
- لها حجم ثابت، لكن شكل غير ثابت (تأخذ شكل الإناء).
- توصف السوائل والغازات بالموائع لأن لها القدرة على الجريان والانسياب.
المائع: هو المادة التي لها القدرة على الجريان أو الانسياب، وتأخذ شكل الإناء الموجودة فيه.
أنواع قوى التجاذب بين الجزيئات:
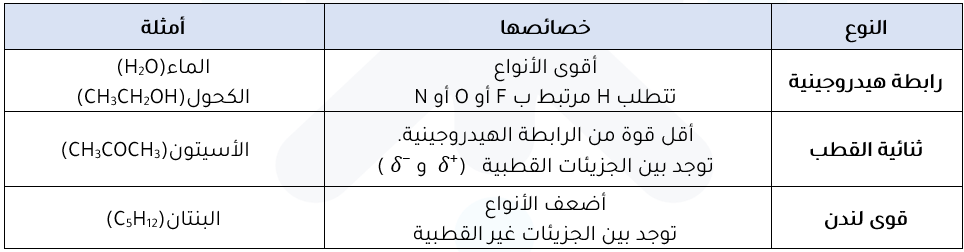
أهم خصائص السوائل:
1- التبخر
2- التكاثف
3- الضغط البخاري
4- درجة الغليان
أولاً: التبخر
تحوّل المادة من الحالة السائلة إلى الحالة الغازية.
يحدث عند أي درجة حرارة عندما تمتلك بعض الجزيئات طاقة حركية كافية لتفلت من سطح السائل.
العوامل المؤثرة على سرعة التبخر:
1- قوى التجاذب بين الجزيئات:
قوى التجاذب بين الجزيئات أكبر سرعة التبخر أقل
2- درجة الحرارة:
درجة حرارة أعلى طاقة حركية أعلى تبخر أسرع
3- طاقة التبخر المولية ∆Hvap:
قوى التجاذب بين الجزيئات أكبر طاقة التبخر المولية أكبر
ثانياً: التكاثف
هي عملية تحول المادة من الحالة الغازية إلى الحالة السائلة.
يحدث عندما تنخفض درجة الحرارة، فتقل الطاقة الحركية للجزيئات وتقترب من بعضها متحولة إلى الحالة السائلة.
ملاحظات:
- طاقة التكاثف = طاقة التبخر
- إذا كانت ∆H في النواتج يكون التفاعل طارد للطاقة.
- إذا كانت ∆H في المتفاعلات يكون التفاعل ماص للطاقة.
ثالثاً: الضغط البخاري
الضغط الناتج عن جزيئات البخار التي تؤثر على سطح السائل في وعاء مغلق عند الاتزان.
العلاقة مع التبخر والتكاثف:
عند الاتزان: سرعة التبخر = سرعة التكاثف.
العوامل المؤثرة في الضغط البخاري:
1- درجة الحرارة
زيادة درجة الحرارة زيادة في الضغط البخاري
2- قوى التجاذب بين الجزيئات
قوى التجاذب بين الجزيئات أقوى الضغط البخاري أقل
رابعاً: درجة الغليان
هي درجة الحرارة التي يتساوى فيها الضغط البخاري للسائل مع الضغط الخارجي الواقع عليه.
درجة الغليان المعيارية: هي درجة الحرارة التي يصبح عندها الضغط البخاري للسائل مساوياً للضغط الجوي(1 atm, 760 mmHg).
- تعتمد درجة الغليان على قوى التجاذب بين جزيئات السائل وتزداد بزيادتها.
قوى التجاذب بين الجزيئات أكبر درجة الغليان أكبر