الحالة السائلة Liquid’s State
الحالة السائلة: هي إحدى حالات المادة الأربع الأساسية، وتتميّز بأنّ لها حجم ثابت وشكل غير ثابت، حيث تأخذ شكل الإناء الذي توضع فيه.
بعض الخصائص الفيزيائية للسوائل:
ترتبط جزيئات المواد المختلفة سواء في الحالة السائلة أو الصلبة بقوى تُسمى قوى التجاذب بين الجزيئات. هذه القوى تؤثر على سلوك المادة وتُفسّر خصائصها الفيزيائية.
هناك ثلاثة أنواع من قوى التجاذب بين الجزيئات منها:
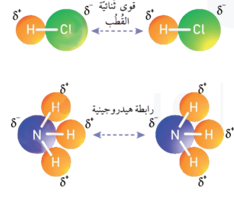
1- الرابطة الهيدروجينية:
- تحدث عندما ترتبط ذرة هيدروجين برابطة تساهمية مع ذرات ذات سالبية كهربائية عالية.
مثل: الفلور (F)، الأوكسجين (O) أو النيتروجين (N)
- وتُعد من أقوى أنواع قوى التجاذب بين الجزيئات.
- قوى ثنائية القطب:
- توجد بين الجزيئات القطبية.
- تنشأ عندما ترتبط ذرة تحمل شحنة جزئية موجبة(𝛿⁺) في جزيء بذرة تحمل شحنة جزئية سالبة (𝛿⁻) من جزيء آخر.
تعتبر أقل قوة من الرابطة الهيدروجينية
3- قوى لندن:
- توجد بين الجزيئات غير القطبية
- تنشأ نتيجة الاستقطاب اللحظي للذرات أو الجزيئات.
تُعتبر أضعف أنواع قوى الترابط بين الجزيئات، لكنها تزداد قوتها بزيادة الكتلة المولية للجزيئات
تذكر أن: السائل مادة ذات حجم ثابت ويأخذ شكل الإناء الذي يوضع فيه.
لفهم خصائص السوائل يجب النظر إلى:
- حركة الجزيئات داخل السائل.
- قوى التجاذب التي تربط بين الجزيئات.
لماذا يطلق على كل من السوائل والغازات اسم الموائع؟
توصف السوائل بأن جزيئاتها تتحرك حركة مستمرة وعشوائية تشبه حركة جزيئات الغازات، ولهذا يُطلق على كل من السوائل والغازات اسم الموائع، نظرًا لقدرتهما على الجريان والانسياب.
المائع: هو المادة التي لها القدرة على الجريان أو الانسياب، وتأخذ شكل الإناء الموجودة فيه.
من ميزات المادة السائلة انها تربط جزيئات السائل بقوى تجاذب ضعيفة نسبيًا تجعلها أكثر تقارباً مما يؤدي إلى:
- كثافة أكبر من كثافة الغازات.
- يجعلها غير قابلة للانضغاط.
- طاقة حركية أقل من جسيمات الغاز.
أهم خصائص السوائل:
1- التبخر
2- التكاثف
3- الضغط البخاري
4- درجة الغليان
أولاً: التبخر
يعرف التبخر بأنه عملية تحول المادة من الحالة السائلة إلى الحالة الغازية.
وحتى تحدث عملية التبخر يجب أن تكون الطاقة الحركية لبعض الجزيئات كافية للتغلب على قوى التجاذب بينها وبين الجزيئات المحيطة بها فتفلت الجزيئات من سطح السائل إلى الحالة الغازية.
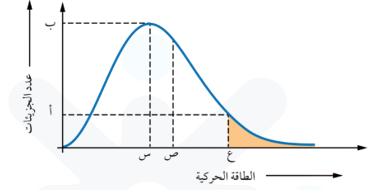
يوضّح الشكل توزيع الطاقة الحركية لجزيئات السائل عند درجة حرارة معينة؛ حيث تمثل الرموز (س، ب، ص، ع، أ) ما يأتي:
س: الطاقة الحركية التي يمتلكها أكبر عدد من جزيئات السائل.
ب: عدد الجزيئات التي تمتلك الطاقة الحركية (س).
ص: متوسط الطاقة الحركية للجزيئات.
ع: الحد الأدنى من الطاقة الحركية اللازمة للتغلّب على قوى التجاذب بين جزيئات السائل.
أ: عدد الجزيئات التي تمتلك الطاقة الحركية (ع).
أما المنطقة المظللة فتمثل الجزيئات التي تمتلك طاقة كافية للتبخر.
كيف تحدث عملية التبخر؟
الاحظ من المنحنى وجود بعض الجزيئات في السائل تمتلك طاقة حركية كافية تجعلها قادرة على التبخر.
وهذه الطاقة تنتج عن الحركة المستمرة والتصادمات المتكررة بين الجزيئات داخل السائل.
فعندما تصطدم الجزيئات ببعضها، تكتسب بعض الجزيئات طاقة إضافية، مما يزيد من سرعتها، ويمنحها القدرة على التحرر من قوى التجاذب التي تربطها بالجزيئات الأخرى.
وعندما تتغلب على هذه القوى، تستطيع أن تفلت من سطح السائل، أي أنها تتبخر.
وهذا ما يفسّر كيف تحدث عملية التبخر من سطح السائل عند أي درجة حرارة، لأن هناك دائمًا بعض الجزيئات التي تمتلك طاقة كافية للهروب والتبخر في أي لحظة.
العوامل المؤثرة في سرعة التبخر:
1- قوى التجاذب يبن الجزيئات
تختلف السوائل في سرعة تبخرها اعتماداً على قوى التجاذب بين جزيئاتها عند ثبات درجة الحرارة.
- يبين الجدول التالي نوع قوى التجاذب بين جزيئات سائلين؛ كحول الإيثانول والأسيتون, ومقارنة بين سرعة تبخرهما.

عند مقارنة نوع قوى التجاذب بين الإيثانول والأسيتون، نجد أن:
- جزيئات كحول الإيثانول ترتبط بروابط هيدروجينية قوية نسبيًا.
- بينما الأسيتون يحتوي على قوى تجاذب ثنائية القطب أضعف.
- بما أن الإيثانول يحتوي على قوى تجاذب أقوى فإن الحد الأدنى من الطاقة اللازمة لتبخر الإيثانول تكون أكبر، لذلك تكون سرعة تبخره اقل.
- وبما أن الأسيتون يحتوي على قوى تجاذب أضعف فإن الحد الأدنى من الطاقة اللازمة لتبخر الأسيتون تكون أقل، لذلك يتبخر أسرع.
الخلاصة: كلما كانت قوى التجاذب بين جزيئات السائل أقوى كان الحد الأدنى من الطاقة اللازمة لتبخره أكبر وسرعة تبخره أقل والعكس.

√أتحقق: أرتب السوائل الآتية تصاعدياً تبعاً لتزايد سرعة تبخرها:
CH3CH3, CH3OH, CH3Cl
الحل: كلما زادت قوى التجاذب بين الجزيئات، قلت سرعة التبخر.
الرابطة الهيدروجينية < ثنائية القطب < قوى لندن
تحليل المركبات:
- CH₃OH يحتوي على أكسجين مرتبطة مباشرة بالهيدروجين إذن رابطة هيدروجينية.
- CH₃Cl جزيء قطبي إذن رابطة ثنائية القطب.
- CH₃CH₃ جزيء غير قطبي إذن قوى لندن.

2- درجة الحرارة :
في الشكل يستخدم منحنى توزيع الطاقة الحركية لجزيئات السائل عند درجتي حرارة T1 و T2 حيث أن T2 > T1 ، والرمز (ع) يمثل الحد الأدنى من الطاقة اللازمة للتبخر ولا يعتمد على درجة الحرارة
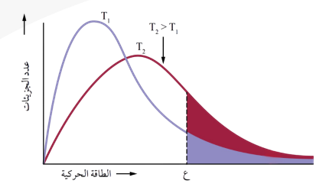
عند مقارنة المساحة المظللة تحت المنحنيين نجد أن:
عدد الجزيئات التي تمتلك الطاقة اللازمة للتبخر عند درجة حرارة T2 أكبر منها عند T1
تفسير ذلك:
زيادة درجة الحرارة تزيد من الطاقة الحركية للجزيئات وتزيد من عدد التصادمات بينها، فيزداد عدد الجزيئات التي تمتلك الحد الأدنى من الطاقة اللازمة للتبخر وتزداد سرعة التبخر.
 3- طاقة التبخر المولية: هي كمية الطاقة اللازمة لتحويل مول واحد من المادة من الحالة السائلة إلى الحالة الغازية عند درجة حرارة معينة.
3- طاقة التبخر المولية: هي كمية الطاقة اللازمة لتحويل مول واحد من المادة من الحالة السائلة إلى الحالة الغازية عند درجة حرارة معينة.
ويمكن تمثيل عملية تبخر مول من الماء بالمعادلة:

تمثل الطاقة في المعادلة طاقة التبخر المولية للماء.
- يوضح الجدول طاقة التبخر المولية لعدد من السوائل عند درجة غليان.
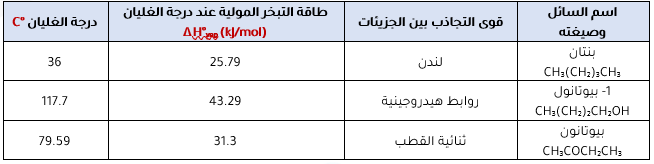
نلاحظ من الجدول تزايد طاقة التبخر المولية للسائل بزيادة قوى التجاذب بين جزيئاته.

أفكر: يمثل الشكل الآتي توزيع الطاقة الحركية لجزيئات سائلين A و B عند درجة حرارة معينة.
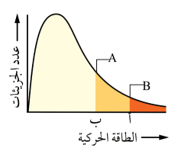
أ: الحد الأدنى من الطاقة اللازمة للتغلب على قوى التجاذب بين جزيئات السائل B فيتبخر.
ب: الحد الأدنى من الطاقة اللازمة للتغلب على قوى التجاذب بين جزيئات السائل A فيتبخر.
- أي السائلين أسرع تبخراً عند درجة الحرارة نفسها؟
السائل B أسرع تبخراً، لأن الطاقة الحركية للسائل B أكبر من الطاقة الحركية للسائل A.
أفكر: أفسر، بالاستعانة بالشكل الآتي الذي يمثل منحنى تسخين الماء:
الحروق الناجمة عن بخار الماء أشد من تلك الناجمة عن الماء الساخن عند 100 ºC.
الإجابة: 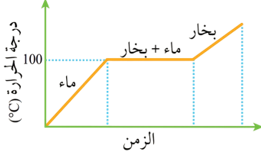
نُلاحظ من المنحنى أن درجة حرارة الماء ترتفع تدريجيًا نتيجة التسخين حتى تصل إلى 100 ºC ، ثم تبقى ثابتة لفترة زمنية على الرغم من استمرار التسخين. خلال هذه المرحلة، يمتص الماء طاقة حرارية إضافية تُستخدم في التغلب على قوى التجاذب بين الجزيئات، مما يؤدي إلى تحوّله إلى بخار.
وبالتالي، فإن بخار الماء يحتوي على طاقة حرارية أكبر تفوق تلك الموجودة في الماء عند 100 ºC. وعند تكاثف البخار على الجلد، يُطلق هذه الطاقة الكامنة بشكل مفاجئ، مما يؤدي إلى حروق أشد من تلك التي يسببها الماء الساخن عند نفس الدرجة.
ثانياً: التكاثف
يعرف التكاثف بأنه عملية تحول المادة من الحالة الغازية إلى الحالة السائلة.
متى تحدث عملية التكاثف؟
تحدث عندما تنخفض درجة حرارة البخار فتقل الطاقة الحركية لجزيئاته وتقل سرعتها، وعندما تتقارب للحد الكافي تتجاذب متحولةً إلى الحالة السائلة.
ماذا ينجم عن عملية التكاثف؟
ينجم عن عملية التكاثف تحرر كمية من الطاقة مساوية لكمية الطاقة الممتصة عند التبخر.
طاقة التكاثف المولية: هي كمية الطاقة الناتجة من تكاثف مول واحد من بخار المادة من الحالة الغازية إلى الحالة السائلة عند درجة حرارة معينة.
ويمكن التعبير عن عملية تكاثف مول من بخار الماء بالمعادلة:
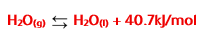
هنا نلاحظ أن طاقة التبخر المولية للماء تساوي طاقة تكاثفه المولية، وأن عملية التبخر ماصة للطاقة وعملية التكاثف طاردة لها.
كيف يمككنا معرفة أن التفاعل ماص ام طارد للحرارة؟
في هذه الحالة دائماً ننظر إلى قيمة ∆H)) إذا كانت بالمتفاعلات يكون التفاعل ماص للطاقة أما إذا كانت بالنواتج يكون التفاعل طارد للطاقة.
√أتحقق: أفسر حدوث عملية التكاثف؟
تحدث عندما تنخفض درجة حرارة البخار فتقل الطاقة الحركية لجزيئاته وتقل سرعتها، وعندما تتقارب للحد الكافي تتجاذب متحولةً إلى الحالة السائلة.
ثالثاً: الضغط البخاري
يعرف الضغط البخاري للسائل بأنه الضغط الناجم عن جزيئات بخار السائل والمؤثر في سطحه عند الاتزان عند درجة حرارة معينة.
عند وضع سائل في وعاء مكشوف، فإنه يستمر بالتبخر.
لكن ماذا يحدث عند وضع السائل في وعاء مغلق؟
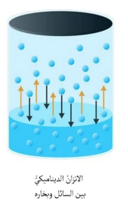
أولاً: يبدأ بالتبخر بحيث تفلت من سطحه الجزيئات ذات الطاقة الحركية العالية.
ثانياً: بمرور الوقت يزداد عدد جزيئات بخار السائل داخل الوعاء، ويزداد تصادمها مع بعضها ومع جدار الوعاء وسطح السائل.
ثالثاً: نتيجة لتلك التصادمات تفقد الجزيئات جزءاً من طاقتها الحركية فتتكاثف.
رابعاً: بمرور الوقت يزداد عدد الجزيئات المتكاثفة حتى يصبح مساوياً لعدد الجزيئات المتبخرة خلال وحدة الزمن، أي أن:
عدد الجزيئات التي تتبخر = عدد الجزيئات التي تتكاثف.
إذن: سرعة التبخر = سرعة التكاثف وهذا يسمى الاتزان الديناميكي.
عندها يسمى الضغط الناجم عن جزيئات بخار السائل والمؤثر في سطحه عند الاتزان عند درجة حرارة معينة الضغط البخاري للسائل.
العوامل التي تؤثر في الضغط البخاري للسائل.
- درجة الحرارة.
- قوى التجاذب بين الجزيئات.
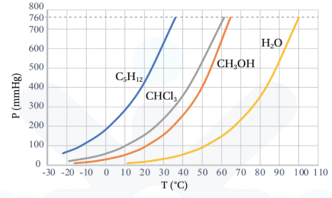
يبين الشكل تغير الضغط البخاري لأربعة سوائل:
البنتان C5H12 ، وثلاثي كلورو ميثان CHCl3 ، الميثانول CH3OH والماء H2O. مع زيادة درجة الحرارة.
تبين أن كلما ازدادت درجة الحرارة ازداد الضغط البخاري للسائل.

بعد ذلك، لمعرفة أثر قوى التجاذب بين جزيئات السائل في ضغطه البخاري؛ نقوم بملاحظة قيم الضغط البخاري للسوائل الأربعة عند درجة الحرارة نفسها، ونوع قوى التجاذب بين جزيئات كل سائل.
- وذلك من خلال الجدول التالي:
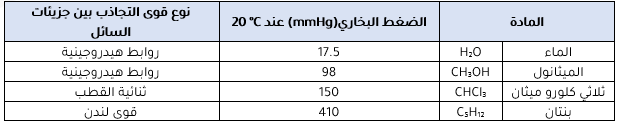
نلاحظ من الجدول أن:
1- الماء H2O :
تترابط جزيئاته بروابط هيدروجينية قوية وله أقل ضغط بخاري، وذلك لأن الحد الأدنى من الطاقة اللازمة للتغلب على قوى الترابط بين جزيئاته أكبر عند درجة حرارة معينة.
2- الميثانول CH3OH:
عدد الروابط الهيدروجينية التي يصنعها الميثانول أقل منها للماء، لذلك؛ فضغطه البخاري أعلى.
3- ثلاثي كلورو ميثان CHCl3:
جزيئات ثلاثي كلورو ميثان تترابط جزيئاته بقوى ثنائية القطب وضغطه البخاري أعلى من الميثانول.
4- البنتان C5H12:
البنتان تترابط جزيئاته بقوى لندن الضعيفة وله أعلى ضغط بخاري.
إذن نلاحظ أنه كلما كانت قوى التجاذب بين جزيئات السائل أقوى قل ضغطه البخاري والعكس.

تدريب: مستعيناً بالشكل (19)، أحدد الضغط البخاري لكل من ثلاثي كلوروميثان والماء عند درجة 50 ºC ، وأقارنها بقيمة ضغطه البخاري الواردة في الجدول (3). ماذا أستنتج؟
الإجابة:
الضغط البخاري لثلاثي كلوروميثان: 500 mmHg
الضغط البخاري للماء: mmHg100
عند مقارنة الضغط البخاري لكل من ثلاثي كلوروميثان والماء عند درجة حرارة 50 ºC
و 20 ºC نلاحظ أن كلما زادت درجة الحرارة زاد الضغط البخاري للسائل.
أفكر: أرتب السوائل الآتية حسب تزايد ضغطها البخاري عند درجة الحرارة نفسها:
CH3CH3, CH3OH, CH3F
الحل: كلما زادت قوى التجاذب بين الجزيئات، انخفض الضغط البخاري.
الرابطة الهيدروجينية < ثنائية القطب < قوى لندن
تحليل المركبات:
- CH₃OH يحتوي على أكسجين مرتبطة مباشرة بالهيدروجين إذن رابطة هيدروجينية.
- CH₃F جزيء قطبي إذن رابطة ثنائية القطب.
- CH₃CH₃ جزيء غير قطبي إذن قوى لندن.

√أتحقق: أفسر تزايد الضغط البخاري للسائل بزيادة درجة حرارته.
الإجابة:
يزداد الضغط البخاري بزيادة درجة الحرارة وذلك لزيادة عدد الجزيئات التي تمتلك الحد الأدنى من الطاقة اللازمة للتبخر فتزداد سرعة التبخر ويزداد عدد الجزيئات المتبخرة والمؤثرة في وحدة المساحة من سطح السائل فيزداد الضغط البخاري.
رابعاً: درجة الغليان
هي درجة الحرارة التي يتساوى فيها الضغط البخاري للسائل مع الضغط الخارجي الواقع عليه، وعندها يبدأ السائل بالغليان وتتكوّن فقاعات في جميع أجزائه.
درجة الغليان المعيارية: هي درجة الحرارة التي يصبح عندها الضغط البخاري للسائل مساوياً للضغط الجوي(1 atm, 760 mmHg).
ملاحظة: تعتمد درجة الغليان على قوى التجاذب بين جزيئات السائل وتزداد بزيادتها.

أفكر: أحدد أي السائلين NH3 أم HF له أعلى درجة غليان.
الإجابة:
HF: يحتوي على ذرة فلور ذات كهروسالبية عالية ويشكّل رابطة هيدروجينية قوية.
NH3: يحتوي على ذرة نيتروجين، وتشكل رابطة هيدروجينية، لكنها أضعف من تلك في HF بسبب الكهروسالبية الأقل للنيتروجين مقارنة بالفلور.
إذن؛ HF له درجة غليان أعلى من NH₃
√أتحقق:
- اعتمادًا على الجدول (3)؛ أستنتج درجة غليان الماء عندما يبلغ الضغط المؤثر على سطحه 355 mmHg
الإجابة: درجة غليان الماء 80 ºC
- اعتمادًا على الشكل (19) ، أحدد درجة الغليان المعيارية لثلاثي كلورو ميثان والبنتان والميثانول.
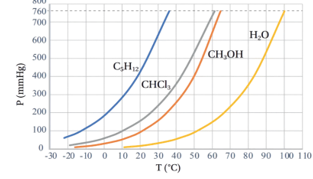
الإجابة:
- درجة الغليان المعيارية لثلاثي كلوروميثان 61 ºC
- درجة الغليان المعيارية للبنتان 36 ºC
- درجة الغليان المعيارية للميثانول 65 ºC