- تمكن بور من تفسير الطيف الذري للهيدروجين، لكنه لم يتمكن من تفسير أطياف العناصر الأخرى لذلك : توالت تجارب العلماء لمعرفة طبيعة الإلكترون
- توصل العالم الفرنسي دي برولي إلى وجود خصائص مزدوجة للإلكترون (موجية – مادية )
- وضع العالم النمساوي شرودنجر تصورًا جديدًا عن حركة الإلكترون الموجية حول النواة، سمّاه ( النموذج الميكانيكي الموجي للذرة ) و أشار إلى أن أكبر إحتمال لوجود الإلكترون هو: ( في منطقةٍ حول النواة تشبه السحابة، أطلق عليها اسم (الفلك )
1) عدد الكم الرئيس (n) Principal Quantum Number
- يشير هذا العدد إلى :
رقم الغلاف الرئيس (مستوى الطاقة الرئيس ) ومعدل بعده عن النواة
- يأخذ هذا الرقم قيما صحيحة موجبة (n= 1, 2, 3, 4,.........,∞)
- يدل كل رقم من هذه الأرقام على غلاف رئيس معين (مستوى طاقة رئيس ) حيث أن :
(n= 1) أقربها للنواة وأقلها طاقة .
- كلما ازدادت قيمة (n) ازداد بعد المستوى عن النواة وازداد حجمه وطاقته.
- إن عدد الكم الرئيس يرتبط بــ :
أ) حجم المستوى ب) معدل بعده عن النواة
2) عدد الكم الفرعي ( ℓ) Lateral Quantum Number
- يمثل هذا العدد الأغلفة الفرعية التي توجد في الأغلفة الرئيسية والتي يساوي عددها قيمة n ضمن الغلاف الرئيس الذي توجد فيه
- عدد الكم الفرعي (ℓ ( = (0, 1, 2, 3, ............, n-1) حيث أن:
الغلاف الرئيس ( n = 1) يتكون من مستوى فرعي واحد يرمز له بالحرف s
الغلاف الرئيس (n = 2) يتكون من مستويين فرعيين يرمز لأحدهما بالرمز s والأخر بارمز p
الغلاف الرئيس ( n = 3) يتكون من ثلاث مستويات فرعية يرمز لها بالرمز (s, p, d)
الغلاف الرئيس ( n = 4) يتكون من أربع مستويات فرعية يرمز لها بالرمز (s, p, d, f)
|
عدد الكم الرئيس (n) |
عدد الكم الفرعي |
رمز الغلاف الفرعي |
|
|
ℓ |
الرمز |
||
|
1 |
0 |
s |
1s |
|
2 |
0 |
S |
2s |
|
3 |
0 |
S |
3s |
|
4 |
0 |
S |
4s |
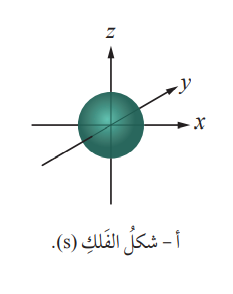
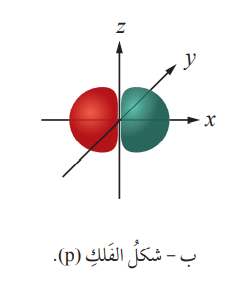
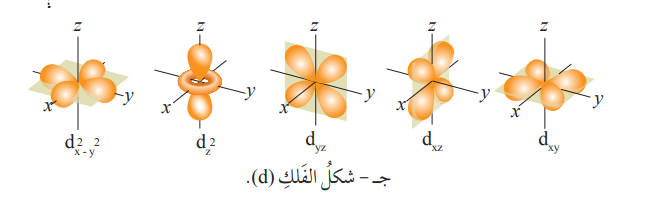
شكل المستوى الفرعي (s) : شكل المستوى الفرعي (p) : شكل المستوى الفرعي (d) :
3) عدد الكم المغناطيسي ( ℓm) Magnetic Quantum Number
- يمثل هذا العدد عدد الأفلاك التي يتكون منها الغلاف الفرعي الواحد
- يرتبط هذا العدد بتحديد الإتجاه الفراغي للفلك ويأخذ قيمًا من (-ɭ إلى +ɭ ) مرورًا بالصفر
- مثال :
- المستوى الفرعي (s) : يتكون من فلك واحد قيمة mɭ له تساوي صفر
- المستوى الفرعي (p) : تكون قيمة (ɭ) له تساوي (1) فيتكون من ثلاث أفلاك (Px, Py, Pz) تتشابه في شكلها وحجمها وطاقتها ضمن الغلاف الرئيس n نفسه ، وقيمة (mɭ) له تساوي (+1, 0 ,-1) ؛ لكن هذه الأفلاك تختلف في إتجاه محاورها حول النواة حيث أنها تأخذ إتجاه المحاور الثلاث (z, y, x) أي أن بعضها متعامد على بعض .
- المستوى الفرعي (d): يتكون من خمس أفلاك قيمُها الكمية (-2, -1, 0, +1, +2)
- المستوى الفرعي (f): يتكون من سبعة أفلاك قيمُها الكمية (-3, -2, -1, 0, +1, +2, +3)
4) عدد الكم المغزلي (ms) Spin Quantum Number
أضيف هذا العدد إلى أعداد الكم الثلاث التي نتجت من حل معادلة شرودنجر.
- يشير هذا العدد إلى إتجاه الدوران (أو غزل) الإلكترون، إذ يدور الإلكترون حول نفسه فضلًا عن دورانه حول النواة
- يأخذ هذا العدد القيم
- عند وجود الكترونين في الفلك نفسه، فإن كلًا منهما سيدور حول نفسه بإتجاه معاكس لدوران الإلكترون الآخر، وينشأ عن ذلك تولد مجالين مغناطيسيين متعاكسين في الإتجاه، ومتجاذبين مغناطيسيًا مما يقلل التنافر الكهربائي بين الإلكترونين.
- مبدأ باولي للإستبعاد :
ينص على " عدم وجود إلكترونين في الذرة نفسها، لهما نفس قيم أعداد الكم الأربعة"
حيث أنه : لا بد أن يختلفا الإلكترونين في عدد كم واحد على الأقل
بناءً على ذلك : يمكن إستنتاج أن الفلك الواحد لا يستوعب أكثر من إلكترونين
- السعة القصوى من الإلكترونات التي يستوعبها المستوى الرئيس (n) = 2n2
- مثلًا: السعة القصوى من الإلكترونات للمستوى الرئيس الثالث (n = 3) هي (2 x 32) وتساوي 18 الكترونًا