الدرس الأول : الحـــالـــة الــغــازيــــة
بعض الخصائص الفيزيائية للغازات Some Physical Properties of Gases
1- حجمها يساوي حجم الوعاء الذي توضع فيه
تمتلك المادة في الحالة الغازية خاصية الانتشار التلقائي لأن جزيئاتها متباعدة جدا وقوى التجاذب بينها شبه معدومة ، وبالتالي فانها تنتشر لتاخذ حجم الوعاء الذي توضع فيه ويصبح حجمها يساوي حجم الوعاء الذي توضع فيه .
2- قابلة للانضغاط
وبسبب تباعد جزيئات المادة في الحالة الغازية وضعف قوى التجاذب بينها فانه يمكن تقليل حجمها من خلال زيادة الضغط المؤثر فيها .
3- تتشابه الغازات في سلوكها الفيزيائي
تتشابه الغازات في سلوكها الفيزيائي رغم انها تتكون من جزيئات تختلف في خصائصها ويعود ذلك الى ضعف قوى التجاذب بين جزيئاتها وتباعدها عن بعضها البعض .
بعد دراسة الخصائص الفيزيائية للغازات توصل العلماء بالتجريب الى مجموعة من القوانين سميت قوانين الغازات ؛ اذ وضحت العلاقة بين متغيرات عدة تصف سلوك الغاز المحصور
مثل العلاقة بين ضغط الغاز (P)وحجمه(V) ودرجة حرارته المطلقة (T)وعدد مولاته(n) .
واستطاع العلماء نفسير خصائص الغازات وسلوكها الفيزيائي عن طريق
نظرية الحركة الجزيئية .
نظرية الحركة الجزيئية The Kinetic Molecular Theory
تصف هذه النظرية سلوك الجسيمات المكونة للمادة ، وتفترض هذه النظرية ان جسيمات المادة في حركة دائمة ومستمرة .
وقد فسرت هذه النظرية سلوك المواد الصلبة والسائلة والغازية اعتمادًا على الطاقة الحركية للجسيمات وقوى التجاذب بينها .
سؤال : ما هو المبدأ الذي اعتمدت عليه نظرية الحركة الجزيئية في تفسير سلوك المواد ؟
الجواب : الطاقة الحركية للجسيمات وقوى التجاذب بينها
لفهم سلوك الغازات وخصائصها افترضت نظرية الحركة الجزيئية وجود غاز سمي الغاز المثالي .
الغاز المثالي : هو غاز افتراضي حجم جسيماته يساوي صفرًا وقوى التجاذب بينها معدومة وتنطبق عليه بنود نظرية الحركة الجزيئية وقوانين الغاز.
بنود نظرية الحركة الجزيئية
1-تتكون الغازات من جسيمات (جزيئات أو ذرات) متناهية في الصغر (مهملة الحجم) ومتباعدة جدا؛ أي أن بينها فراغات كبيرة؛ مما يعني أن معظم الحجم الذي يشغله الغاز فراغ. وهو ما يفسر الكثافة المنخفضة للغازات مقارنة بالسوائل والمواد الصلبة، كما يفسر قابلية الغازات للانضغاط بسهولة.
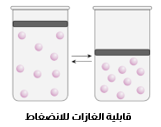
سؤال : فسر ؛ كثافة الغازات اقل من كثافة المواد في الحالتين السائلة والصلبة ؟
الجواب : لأن الغازات تتكون من جسيمات (جزيئات أو ذرات) متناهية في الصغر ومتباعدة جدا؛ أي أن بينها فراغات كبيرة؛ مما يعني أن معظم الحجم الذي يشغله الغاز فراغ .
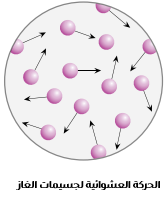
2-تتحرك جسيمات الغاز حركة مستمرة وعشوائية وسريعة في جميع الاتجاهات وبخطوط مستقيمة. وهذا ما يكسبها طاقة حركية تتغلب على قوى التجاذب بينها، وهو ما يفسر انتشار الغازات وتدفقها
3-تتصادم جسيمات الغاز في ما بينها، كما تتصادم مع جدار الإناء الموجودة فيه تصادما مرنا؛ ويكون التصادم مرنا عندما يبقى مجموع الطاقة الحركية للجسيمات ثابت، فالطاقة التي يفقدها أحد الجسيمات يكسبها جسيم آخر عند درجة الحرارة نفسها، يلاحظ من الشكل المجاور أن مجموع الطاقة الحركية يبقى محفوظا في التصادمات المختلفة.
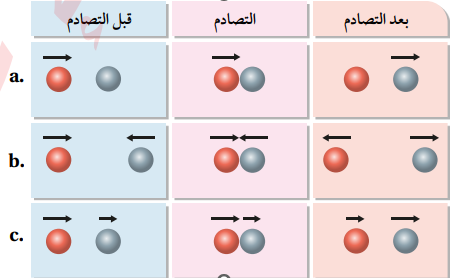
التصادمات المرنة لجسيمات الغاز، ويشير السهم إلى مقدار طاقة كل منها
سؤال : متى يكون التصادم مرناً ؟
الجواب : عندما يبقى مجموع الطاقة الحركية للجسيمات ثابت.
4-قوى التجاذب بين جسيمات الغاز المثالي معدومة؛ لذلك لا يمكن إسالته مهما زاد الضغط المؤثر فيه أو انخفضت درجة حرارته .
**المقصود بإسالة الغاز تحوله الى الحالة السائلة وذلك من خلال زيادة الضغط المؤثر فيه او خفض درجة حرارته فان جزيئاته تنشأ بينها قوى التجاذب بينها و تتقارب من بعضها البعض متحولا الى الحالة السائلة بينما الغاز المثالي فان قوى التجاذب بين جزيئاته معدومة وعليه فانه لا يمكن التاثير فيها بزيادة او بنقصان ولا يمكن اسالته .
سؤال : فسر ؛ كثافة لا يمكن اسالة الغاز المثالي ؟
الجواب : لأن قوى التجاذب بين جسيمات الغاز المثالي معدومة .
5-يعتمد متوسط الطاقة الحركية لجسيمات الغاز على سرعتها التي تزداد بزيادة درجة الحرارة وتقل بنقصانها.
سؤال : على ماذا يعتمد متوسط الطاقة الحركية لجسيمات الغاز ؟
الجواب :يعتمد على سرعه جسيمات الغاز
سؤال : ما العامل المؤثر في سرعة جسيمات الغاز ؟
الجواب :درجة الحرارة ، والعلاقة بينهما طردية ( كلما زادت درجة الحرارة زادت سرعة جسيمات الغاز ،وكلما قلت درجة الحرارة قلت سرعة جسيمات الغاز )
Real Gases الغازات الحقيقية
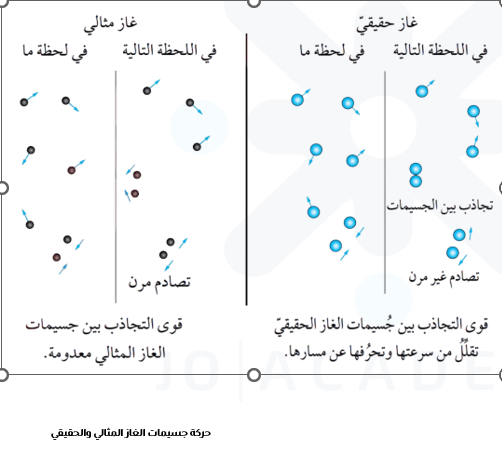
المسافات بين جسيمات الغاز الحقيقي في الظروف العادية كبيرة جدا وقوى التجاذب بينها شبه معدومة، فيكون سلوكها مشابها لسلوك الغاز المثالي. وعند زيادة الضغط المؤثر في الغاز الحقيقي؛ فإن المسافات بين جسيماته تقل وتنشأ بينها قوى تجاذب؛ مما يقلل حركتها العشوائية وسرعتها، فتنحرف عن سلوك الغاز المثالي، وكلما زادت قوى التجاذب بين جسيمات الغازات زاد انحرافها عن سلوك الغاز المثالي، وذلك عند الظروف نفسها من الضغط ودرجة الحرارة لذا؛ تختلف الغازات الحقيقية في سلوكها عن الغاز المثالي، ويزداد اختلافها بزيادة الضغط المؤثر فيها وخفض درجة حرارتها.
فمثلا؛ يتكون غاز الهيليوم من ذرات صغيرة جدا تتجاذب بقوى لندن الضعيفة؛ لذا يشبه في سلوكه الغاز المثالي، وعند زيادة الضغط وخفض درجة الحرارة على نحو كبير؛ فإن ذرات الغاز تتقارب وتقل طاقتها الحركية ويزداد التجاذب في ما بينها، فيتحول الغاز إلى الحالة السائلة.
يوضح الشكل المحاور أثر قوى التجاذب بين جسيمات الغاز الحقيقي في حركة هذه الجسيمات مقارنة بجسيمات الغاز المثالي عند لحظتين متتاليتين.
افكر : اي الغازين تتوقع ان يكون اقرب في سلوكه الى الغاز المثالي عند الظروف نفسها NH3 امNe
Ne اقرب في سلوكه الى الغاز المثالي لان قوى التجاذب بين جزيئاته قوى لندن وهي اضعف من الرابطة الهيدروجينية في NH3
√اتحقق : ما الظروف التي يكون سلوك الغاز الحقيقي عندها أقرب إلى سلوك الغاز المثالي؟
الجواب : يكون سلوك الغاز الحقيقي أقرب إلى سلوك الغاز المثالي عندما تزداد درجة الحرارة ويقل الضغط المؤثر على الغاز،لان قوى التجاذب بين جزيئات الغاز تكون صغيرة عند هذه الظروف ويمكن تجاهلها ..
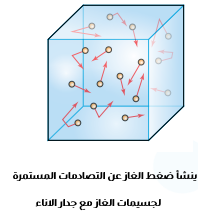
تعلم ان جسيمات الغاز تتصادم مع بعضها البعض ومع جسيمات الوعاء المحصورة فيه بسبب حركتها الدائمة والمستمرة العشوائية ونتيجة تصادمها المستمر بجدار الاناء الداخلي تتولد قوة تؤثر فيه تسمى ضغط الغاز .
ضغط الغاز : القوة المؤثرة في وحدة المساحة .
العوامل المؤثرة في ضغط الغاز :
1- حجم الغاز 2- درجة حرارة الغاز
وحدات قياس الضغط ورموزها والعلاقات بينها :
(atm)ضغط جوي
1 atm = 760 mmHg (mmHg)زئبق مليمتر
1atm = 101.3 kPa (kPa) كيلوباسكال
توضح قوانين الغاز العلاقات الرياضية بين كل من؛ كمية الغاز وحجمه وضغطه ودرجة حرارته
مثال : kPa وبوحدة atm
KPa والى وحدة atm الى وحدةmmHg الحل: المطلوب هو تحويل القيمة المعطاه من وحدة
نستخدم العلاقة : atm الى وحدةmmHg للتحويل من وحدة
1am = 160 mmHg
P( atm )= 798 mmHg x =1.05 atm
نستخدم العلاقة : atm kPa الى وحدة mmHg للتحويل من وحدة
760 mmHg = 101.3 kPa
P( kPa )= 798 mmHg x =106.4 kPa
Boyle's Lawبويل قانون
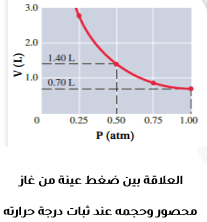
درس العالم بويل العلاقة بين ضغط الغاز المحصور وحجمه عند ثبات درجة حرارته، وتوصل إلى أن مضاعفة ضغط كمية محددة من الغاز المحصور يؤدي إلى نقصان حجمه إلى النصف، وأن إنقاص ضغطه إلى النصف يؤدي إلى زيادة حجمه إلى الضعف ،
نص قانون بويل
«حجم كمية محددة من الغاز المحصور يتناسب عكسياً مع الضغط الواقع عليه عند ثبات درجة حرارته»
يُعبر عن قانون بويل رياضيا على النحو الآتي:
عند ثبات درجة الحرارة، فإن:
V =
مقدار يسمى ثابت التناسب، ومنها:k حيث
P x V= k
P1 x V1=P2 x V2
حيث :
(ml) او المليلتر (L): حجم الغاز ويمكن قياسه بوحدة اللتر V
:ضغط الغاز P
ويمكن تفسير قانون بويل باستخدام نظرية الحركة الجزيئية؛ إذ إن زيادة الضغط المؤثر في الغاز المحصور يؤدي إلى تقارب جسيماته فيقل حجمه ،ويزداد عدد تصادمات جسيمات الغاز مع جدار الإناء فيزداد ضغطه عند ثبات درجة حرارته
مثـــال: عينة من غاز النيتروجين حجمها ml150وضغطها atm0.950 ، احسب حجمها بوحدةml حين يصبح ضغطها مساويا 0.990atm؛ عند درجة الحرارة نفسها
المعطيات : v1=150ml ، p1=0.950، p2=0.990
المطلوب : v2=??
الحــل:
اما لو طلب السؤال ايجاد الحجم بوحدة لتر ، بامكانك قسمة الناتج على 1000 او قسمة v1 على 1000 قبل الاستخدام في الحل فيكون الناتج بوحدة لتر .
√اتحقق : عينة من غاز محصور حجمهاL4 عند ضغط atm2، سمح لها بالتمدد حتى اصبح حجمها L12 احسب ضغطها عند درجة الحرارة نفسها .
المعطيات : v1=4L ، p1=2 atm، V2=12L
المطلوب : P2=??
الحــل:
.
charles's Lawشارل قانون
درس العالم شارل أثر تغيير درجة حرارة الغاز المحصور في حجمه عند ثبات ضغطه، وتوصل إلى أن زيادة درجة حرارة الغاز المطلقة تزيد من حجمه عند ثبات ضغطه؛ فعند زيادتها إلى الضعف - مثلاً - يتضاعف حجمه عند ثبات الضغط،
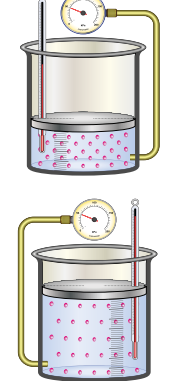
اثر زيادة درجة حرارة الغاز في حجمه عند ثبات ضغطه .
«حجم كمية محددة من الغاز المحصور يتناسب طردياً مع درجة حرارته المطلقة عند ثبات ضغطه »
يُعبر عن قانون شارل رياضيا على النحو الآتي:
عند ثبات الضغط ، فإن:
العلاقة بين الحجم ودرجة الحرارة المطلقة طردية
ومنه
حيث :
: حجم الغاز V
T: درجة الحرارة بالكلفن ويمكن حسابها T(°C) + 273 T (K)=
ويمكن تفسير قانون شارل باستخدام نظرية الحركة الجزيئية؛ حيث إن زيادة درجة حرارة الغاز تزيد من متوسط الطاقة الحركية الجسيماته، فتزداد سرعتها ويزداد عدد تصادماتها، مع جدار الإناء، ولكي يبقى ضغط الغاز المحصور ثابتا؛ فلا بد من زيادة حجمه.
مثـــال: عينة من غاز الاكسجين حجمها L6.82 عند درجة حرارة °C 327، احسب حجمها بوحدةL عند °C 27 بفرض ثبات الضغط .
المعطيات : v1=6.82L ، T1=327°C ، °C T2=27
المطلوب : v2=??
الحــل:
اولا يجب ان تكون درجة الحرارة بوحدة K
T1(°C) + 273 T2 (K)= T2(°C) + 273 T1 (K)=
T1 (K)=327+273=600K T2 (K)= 27+273=300K
لاحظ ان خفض درجة الحرارة ادى الى نقصان حجم الغاز .
ملاحظة: للتمييز بين قانوني بويل وشارل من خلال معطيات السؤال
بويل لم يتعامل مع درجة الحرارة وافترض انها ثابته لكنه تعامل مع الضغط بينما شارل لم يتعامل مع الضغط وافترض انه ثابت وتعامل مع درجة الحرارة
√اتحقق : عينة من غاز النيتروجين حجمها30mL4 عند 24°C ، عند اي درجة حرارة يصبح حجمها L0.75 بفرض ثبات الضغط .
المعطيات : v1=430mL ، T1=24°C ، V2=0.75L
المطلوب : T2=??
اولا يجب ان تكون درجة الحرارة بوحدة K
T1(°C) + 273 T1 (K)=
T1 (K)=24+273=297K
ثانيا يجب ان تكون الحجوم متشابهه الوحدة ) الحجمين باللتر او الحجمين بالملليتر (.
v1=430mL /1000= 0.430L
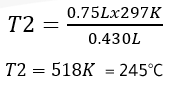
قانون جاي - لوساك Gay -Lussac's Law
درس العالم جاي - لوساك العلاقة بين ضغط الغاز ودرجة حرارته عند ثبات حجمه، وتوصل إلى أن زيادة درجة حرارة كمية محددة من الغاز المحصور تزيد من ضغطه عند ثبات حجمه. يُطلق على هذه العلاقة قانون جاي - لوساك
نص قانون قانون جاي - لوساك
«ضغط كمية محددة من الغاز المحصور يتناسب طردياً مع درجة حرارته المطلقة عند ثبات ضغطه »
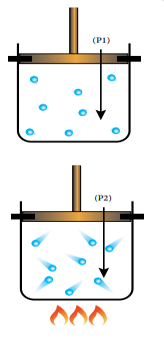
أثر درجة الحرارة في الطاقة الحركية لجسيمات الغاز
تفسر نظرية الحركة الجزيئية قانون جاي لوساك؛ إذ تؤدي زيادة درجة حرارة الغاز إلى زيادة متوسط الطاقة الحركية لجسيماته، ومن ثم تزداد سرعتها ويزداد عدد تصادماتها فيزداد ضغطه عند ثبات حجمه
يُعبر عن قانون جاي - لوساك رياضيا على النحو الآتي:
حيث :
: ضغط الغاز P
T: درجة الحرارة بالكلفن ويمكن حسابها
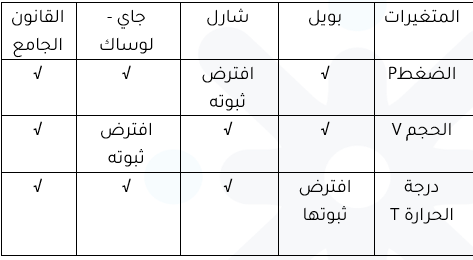
ملاحظة: للتمييز بين قوانين كل من بويل وشارل وجاي – لوساك من خلال معطيات السؤال
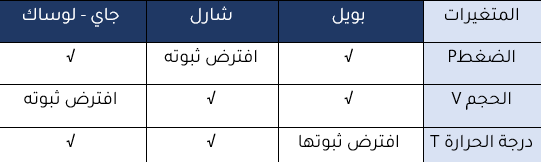
مثـــال: تحمل عبوات الرذاذ، مثل ملطفات الجو ومثبتات الشعر، إشارات تحذر من تسخين العلبة أو تخزينها على درجات حرارة عالية. إذا علمت أن ضغط الغاز داخل إحدى هذه العبوات 775mmHg عند درجة حرارة °C 25 وارتفعت درجة حرارة الجو إلى °C 40 فأحسب ضغط الغاز داخلها
المعطيات : P1=775mmHg ، T1=25°C ، °C T2=40
المطلوب : P2=??
الحــل:
اولا يجب ان تكون درجة الحرارة بوحدة K
T1(°C) + 273 T2 (K)= T2(°C) + 273 T1 (K)=
T1 (K)=25+273=298K T2 (K)= 40+273=313K
القانون الجامع للغازات The Combined Gas Law
يصاحب تغير درجة حرارة الغاز تغير في حجمه وضغطه معا؛ لذلك جمع العلماء قوانين الغاز الثلاثة بويل وشارل وجاي - لوساك، في قانون واحد سمي القانون الجامع للغازات إذ يصف العلاقة بين ضغط كمية محددة من الغاز المحصور وحجمها ودرجة حرارتها .
يُعبر عن قانون جاي - لوساك رياضيا على النحو الآتي:
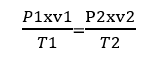
حيث :
: ضغط الغاز P
T: درجة الحرارة بالكلفن
: حجم الغاز v
مثـــال: ، عينة من الهواء حجمهاL5وضغطها mmHg 803عند درجة حرارة °C 25- حرارة الجو إلى °C أحسب ضغطها اذا سخنت حتى اصبح حجمها7L ودرجة حرارتها °C97 .
المعطيات : P1=803mmHg ، T1= -20°C ، T2=97°C V2=7L V1=5L
المطلوب : P2=??
الحــل:
اولا يجب ان تكون درجة الحرارة بوحدة K
T1(°C) + 273 T2 (K)= T2(°C) + 273 T1 (K)=
T1 (K)= -20+273=253K T2 (K)= 97+273=370K
√اتحقق : اذا علمت ان بالونا يحتوي على 50L من غاز الهيليوم عند درجة حرارة 25°C وضغط 1.08atm فاحسب حجمه عند ضغط atm0.8 ودرجة حرارة 10°C.
المعطيات : P1=1.08atm ، T1= 25°C ، T2=10 °C p2=0.8atm V1=50L
المطلوب : v2=??

قانون أفوجادرو Avogadro's Law
تتأثر الخصائص الفيزيائية لكمية محددة من الغاز المحصور بثلاثة عوامل: الحجم، والضغط، ودرجة الحرارة. ولكن، ماذا لو تغيرت كمية الغاز ؟
درس العالم أفوجادرو العلاقة بين حجم الغاز وكميته، وتوصل إلى أن: الحجوم المتساوية من الغازات المختلفة تحتوي العدد نفسه من الجسيمات عند الظروف نفسها من الضغط ودرجة الحرارة، وهو ما يعرف بقانون أفوجادرو
وقد توصل العالم أفوجادرو أيضًا إلى أن حجم المول الواحد من أي الغاز يساوي (22.4L) ويحتوي 1023 × 6.02 من جسيمات هذا الغاز في الظروف المعيارية، وسمي حجم المول الواحد من أي غاز في الظروف المعيارية الحجم المولي للغاز .
وعليه ، فإنه عند مضاعفة عدد مولات الغاز يتضاعف حجمه عند ثبات ضغطه ودرجة حرارته؛ أي أن حجم الغاز المحصور يتناسب طرديا مع عدد مولاته عند ثبات ضغطه ودرجة حرارته،
تفسر نظرية الحركة الجزيئية العلاقة بين حجم الغاز وعدد مولاته؛ إذ إن زيادة عدد مولات الغاز تزيد من عدد جسيماته، ومن ثم يزداد عدد تصادماتها مع جدار الإناء، ولكي يبقى ضغط الغاز ودرجة حرارته ثابتين؛ فلا بد من زيادة حجمه.
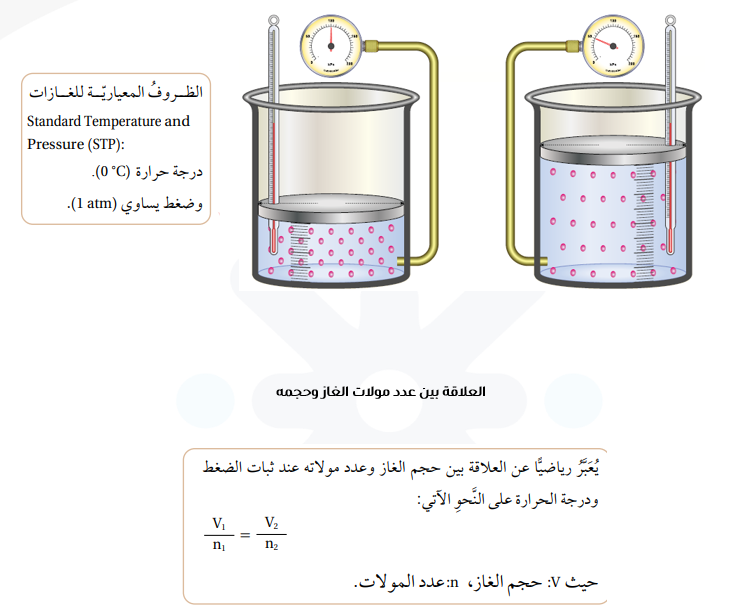
مثـــال: ، إذا علمت أن بالونا حجمهL يحتوي على m 0.1 mol من غاز الهيليوم ضخت داخله كمية إضافية من الغاز فأصبح حجمه L 2.8، فأحسب عدد مولات الغاز بعد الإضافة، بفرض ثبات ضغطه ودرجة حرارته.
المعطيات : ، n1= 0.1 mol ، V2=2.8L V1=2.2L
المطلوب : n2=??
من خلال معطيات السؤال يتبين معنا اي قوانين الغازات نستخدم
فمثلا هذا المثال ذكر عدد المولات والحجم فقط . وعليه فان القانون الذي يربط عدد المولات والحجم معا فقط هو قانون افوجادرو
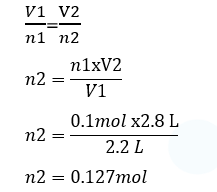
√اتحقق : ما الحجم الذي يشغله mol3.5 من غاز الكلور Cl2 في الظروف المعيارية .
1مول من اي الغاز حجمه22.4 L في الظروف المعيارية وبالتالي فإن حجم 3.5 مول
v2= n xV V2 = 3.5 mol × 22.4 L/mol V2 = 78.4 L
افكر : كيف يتغير ضغط الغاز عند زيادة عدد مولاته مع بقاء حجمه و درجة حرارته ثابتين؟
كلما زاد عدد مولات الغاز يزداد ضغطه والعكس .
قانون الغاز المثالي Ideal Gas Law
ربط العلماء بين ضغط الغاز وحجمه ودرجة حرارته وعدد مولاته بعلاقة رياضية، تعرف بقانون الغاز المثالي ، حيث ينطبق القانون على الغاز المثالي وهو غاز افتراضي، ويمكن تطبيقه على الغازات الحقيقية بافتراض أنها تسلك سلوك الغاز المثالي على النحو الآتي
P V = n R T
حيث P: ضغط الغاز V: حجم الغاز n: عدد المولات R: ثابت الغاز العام
T: درجة الحرارة بالكلفن R: ثابت الغاز العام ويساوي (0.082L.atm/mol.K)
مثـــال: ، احسب الضغط الناجم عن mol 0.45، من غاز ما في وعاء حجمه 1.5L ودرجة حرارته 20°C.
المعطيات : R=0.082L.atm/mol.K ، T= 20°C ، n=0.45mol V=1.5L
المطلوب : P=??
الحل : لاحظ عزيزي الطالب ان معطيات السؤال مهم جدا تحديدا حتى تتمكن من اختيار القانون المناسب من قوانين الغازات لحساب المطلوب .
من خلال معطيات السؤال يتبين لنا ان القانون المستخدم هو قانون الغاز المثالي PV=nRT

√اتحقق : تُعبأ كرات التنس بغاز النيتروجين. أحسب عدد مولات الغاز في كرة حجمها1.5L وضغط الغاز داخلها 2 atm عند درجة حرارة °C25.
المعطيات : R=0.082L.atm/mol.K ، T= 25°C ، p=2 atm V=0.15L
المطلوب : n=??
من خلال معطيات السؤال يتبين لنا ان القانون المستخدم هو قانون الغاز المثالي PV=nRT
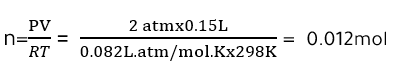
ملاحظة : قيمة R لا تعطى عادة خلال السؤال وانما تعطى بشكل عام بداية صفحة الامتحان ؛ ويفضل حفظها مع وحدتها .
قانون دالتون للضغوط الجزئية Dalton's Law of Partial Pressures
تختلط الغازات بسهولة، وما الرائحة التي نشتها للطعام عند نضجه إلا دليلا على اختلاط أبخرته بالهواء داخل المنزل. وَيُفَسَّر اختلاط الغازات وفق نظرية الحركة الجزيئية؛ بأن جسيمات الغاز متباعدة جدا وفي حركة مستمرة وسريعة وعشوائية؛ مما يجعلها تتحرك وتنتشر في الفراغات بين جسيمات بعضها بعضا مكونة خليطاً من الغازات
درس العالم دالتون الضغط الناجم عن خليط مكون من غازات عدة لا تتفاعل مع بعضها بعضا داخل إناء واحد، ويوضح الشكل المجاور أن الغازين A و B في وعائين منفصلين لهما الحجم نفسه عند درجة الحرارة نفسها، ولكل غاز ضغط خاص به ناجم عن حركة جسيماته المستمرة والعشوائية وتصادمها مع جدار الإناء الموجودة فيه، وعدد جسيمات الغاز A أكبر منها للغاز 8، ومن ثُمَّ فإن ضغطه أكبر، وعند جمع الغازين في وعاء واحد له الحجم نفسه وعند درجة الحرارة نفينها تستمر حركة جسيمات كل غاز ويستمر تصادمها مع جدار الإناء كما لو كانت وحدها فيه وعليه؛ فإن لكل غاز ضغطاً مساويًا لضغطه وهو منفرد، أما الضغط الجديد داخل الإناء فناجم عن الغازين معا، ويساوي مجموع ضغطيهما. يُسمى الضغط الذي يؤثر به الغاز في خليط من الغازات غير المتفاعلة الضغط الجزئي للغاز
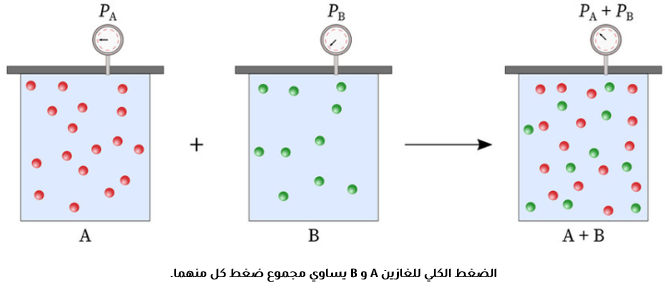
توصل العالم دالتون إلى العلاقة بين الضغط الكلي لخليط من الغازات التي لا تتفاعل مع بعضها بعضا والضغط الجزئي للغازات المكونة للخليط، أطلق عليها قانون دالتون للضغوط الجزئية .
نص قانون دالتون للضغوط الجزئية
« الضغط الكلي لخليط من الغازات التي لا تتفاعل مع بعضها يساوي مجموع الضغوط الجزئية لجميع مكونات الخليط ».
يُعبر عن قانون دالتون رياضيا على النحو الآتي:
PT=PA+PB+PC+………
حيث PT: الضغط الكلي لخليط الغازات PA: الضغط الجزئي للغاز A:
:PB الضغط الجزئي للغاز PC B: الضغط الجزئي للغاز C.
مثـــال: ، أحسب الضغط الكلي لخليط من الغازات مكوّن من غاز النيتروجين الذي ضغطه الجزئي 0.247atm ، وغاز الأكسجين الذي ضغطه الجزئي atm0.346 ، وغاز ثاني أكسيد الكربون الذي ضغطه الجزئي .0.444atm
المعطيات : PCO2 =0.444atm ، PN2 =0.247atm PO2 =0.346atm
المطلوب : PT =??
PT=PN2 +PO2+ PCO2 PT= 0.247 atm+ 0.346 atm + 0.444 atm = 1.037 atm
مثـــال: ، أحسب الضغط الكلي لخليط من الغازات مكوّن من 0.02molغاز الهيليوم He و 0.01mol من غاز الهيدروجين H2 في وعاء حجمه 5L ودرجة حرارته 10°C .
المعطيات : V =5L T= 10°C n He =0.02atm n H2 =0.01atm
المطلوب : PT

ويمكن حساب الضغط الجزئي للغاز بمعرفة الضغط الكلي لخليط الغازات وعدد مولات كل غاز ومنها حساب الكسر المولي للغاز ثم ضغطه الجزئي

مثـــال: خليط من الغازات يحتوي 0.75mol N2 و 0.3mol O2 و 0.15mol CO2 ، اذا كان الضغط الكلي يساوي 1.56atm احسب الضغط الجزئي لكل غاز في الخليط .
المعطيات : nCO2 =0.15mol ، p T =1.56 atm nN2 =0.75mol nO2 =0.3mol
المطلوب : P N2 =?? P O2 =?? P CO2 =??
n T=n N2+n O2+n CO2 n T = 0.75mol + 0.3mol+ 0.15mol n T = 1.2mol
الضغط الجزئي= الكسر المولي x الضغط الكلي .

√اتحقق : خلط 2L من غاز النيتروجين N2 ضغطه atm 0.395 مع 3L من غاز الهيدروجينH2 ضغطه 0.11atm في وعاء واحد حجمه 1L، أحسب الضغط الكلي للخليط عند درجة الحرارة نفسها.
PN2=2 x 0.395 = 0.79 atm
PH2=3 x 0.11 = 0.33 atm
PT=0.79+0.33 = 1.12 atm
√اتحقق : خليط من الغازات يتكون من 5.1g N2، 2.83g H2 ،5.17g NH3 اذا كان الضغط الكلي للخليط يساوي atm 2.35 ، أحسب الضغط الجزئي لكل غاز .
علما أن :
Mr N₂ = 28 g/mol, Mr H₂ = 2 g/mol, MrNH3 = 17 g/mol
الحل :
الضغط الجزئي= الكسر المولي x الضغط الكلي .
نجد الكسر المولي لكل غاز وهو يساوي

الانتشار والتدفق Diffusion and Effusion
تنتشر رائحة العطور في أرجاء المنزل عند رشها، فما تفسير ذلك ؟
تتميز الغازات بخصائص فيزيائية عدة؛ منها الانتشار والتدفق، وَيُعَرَّفُ الانتشار بأنه؛ عملية الاختلاط التدريجي للغازات في ما بينها نتيجة انتقالها من المنطقة الأعلى تركيزا إلى المنطقة الأقل تركيزا، وينسجم ذلك مع نظرية الحركة الجزيئية؛ إذ تحدث عملية الانتشار لأن جزيئات الغاز متباعدة وفي حركة مستمرة وسريعة وعشوائية؛ فيسمح ذلك لها بالاختلاط بغيرها من الغازات.. وَيُعَرَّفُ التدفق بأنه؛ تسرب الغاز المضغوط من فتحة صغيرة في جدار الإناء الموجود فيه، كتسربه من محبسه في المدفأة، وتسرب الهواء من عجل السيارة نتيجة اختراقه بوساطة مسمار مثلا.
درس العالم جراهام انتشار الغازات وتدفقها ، ولاحظ أن الغازات ذات الكتلة المولية الأقل أسرع انتشارًا وتدفّقا من الغازات ذات الكتلة المولية الأكبر. وتوصل إلى أن " سرعة تدفق الغاز يتناسب عكسياً مع الجذر التربيعي لكتلته المولية عند درجة حرارة وضغط ثابتين" وهو ما يُعرَفُ بقانون جراهامولن يتم التطرق للحسابات الخاصة بتطبيق هذا القانون..
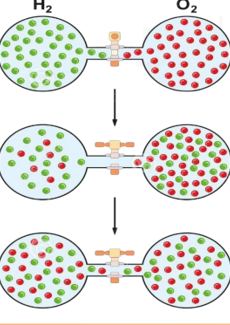
يبين الشكل المجاور تدفق غازي الهيدروجين والأكسجين عند فتح الصمامبين الغازين، إذ إن تدفق جزيئات غاز الهيدروجين أسرع من جزيئات غاز الأكسجين؛ حيث ينتقل عدد أكبر من جزيئات غاز الهيدروجين عبر الصمام مقارنة بعدد جزيئات غاز الأكسجين التي تنتقل بالاتجاه الآخر ومع الوقت يختلط الغازان تماما