- مفاهيم الحموض والقواعد:
- ما هو الحمض؟
هي مادة تنتج ايون
- مثال : معادلة تفكك الحمض الافتراضي HA.
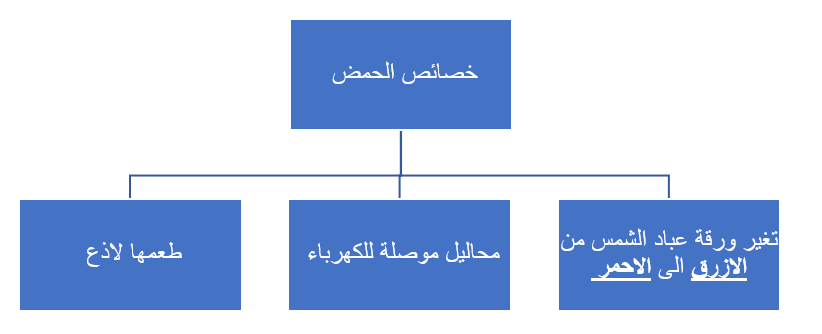
- تقسم الاحماض الى نوعين : 1- الاحماض القوية 2- الاحماض الضعيفة.
سؤال: ما هي الحموض القوية ؟
- هي حموض تتفكك كلياً بالماء 2- تفاعلها غير منعكس (اي باتجاه واحد).
- مثال : على الأحماض القوية .(مهم).
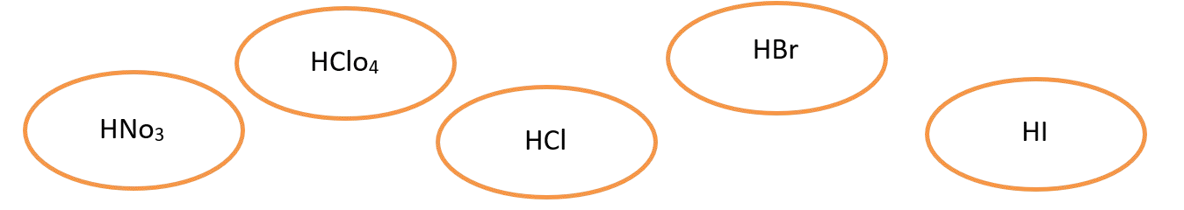
سؤال: ما هي الحموض الضعيفة ؟
- هي حموض تتفكك جزئياً بالماء 2- تفاعلها منعكس ( اي بانها باتجاهين).
- مثال: على الاحماض الضعيفة (مهم) :
- اي مركب يبدأ ب H باستثناء (الحموض القوية ) مثل HCN .
- اي مركب ينتهي ب OOH مثل HCOOH .
- ما هي القاعدة؟
هي مادة تنتج ايون عند تاينها في الماء او ايون موجب اخر.
- مثال : معادلة تفكك القاعدة .
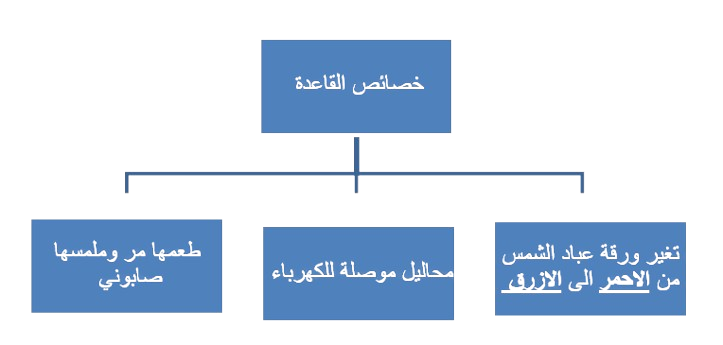
- تقسم القواعد الى نوعين :
- القواعد القوية. 2- القواعد الضعيفة.
سؤال : ما هي القواعد القوية ؟
- هي قواعد تتفكك كلياً بالماء 2- تفاعلها غير منعكس (اي باتجاه واحد).
- مثال: على القواعد القوية (مهم) :
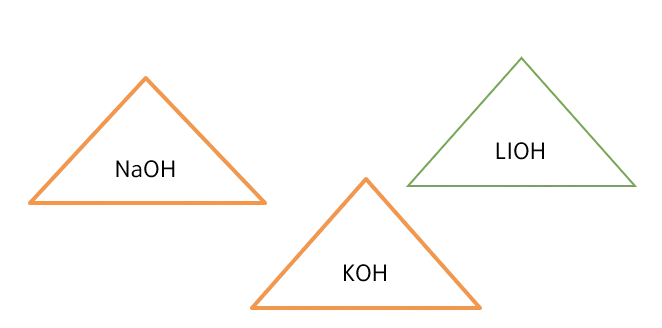
- اولاً : مفهوم ارهينيوس .
تمكن العالم ارهينيوس عن طريق دراسته التوصيل الكهربائي لمحاليل المواد الايونية من وضع تصور حول مفهوم الحمض والقاعدة ، وقد عدت هذة خطوة رائدة في مجال الكيمياء والتحليل الكيميائي . فما المقصود بالحمض والقاعدة حسب مفهوم ارهينيوس؟
حمض ارهينيوس : مادة تتأين في الماء وتنتج ايون الهيدروجين .
بعض الحموض تحتوي على ذرة هيدروجين واحدة ، مثل (HCl) ،ويسمى حمضا احادي البروتون .
وبعضها يحتوي على ذرتي هيدروجين مثل حمض الكبرتيك
وبعضها يحتوي على ثلاث ذرات هيدروجين مثل حمض الفسفوريك
- مهم: في الحموض الكربوكسلية ذات الصيغة ومثال عليها RCOOH :
السبب في تأين ذرة الهيدروجين في الحمض ان ذرة الهيدروجين نرنبط برابطة قطبية تساهمية ذات كهروسلبية عالية ومجموعة ايونية
تتاين HCOOH لا تتأين ,
- أوجه قصور ارهينيوس:
- فسر الحموض والقواعد في المحاليل المائية فقط.
- لم يتمكن من تفسير التاثير القاعدي لقواعد معروفة مثل (NH3 )
- لم يتمكن من تفسير التاثير القاعدي او الحمضي لمحاليل الاملاح.
- ايون الهيدروينيوم:
- جسيم حجمه
- صغير جدا.
- يحمل شحنة كهربائية عالية جداً ( ذو كثافة كهربائية عالية).
- ثانياً: مفهوم برونستد – لوري.
تمكن العالمان برونستد، ولوري من وضع تصور جديد لمفهومي الحمض والقاعدة بالاعتماد على انتقال
البروتون ( H+ ) من الحمض الى القاعدة في اثناء التفاعل .
قالحمض : مادة قادرة على منح البروتون ( ( H+ اثناء التفاعل (مانح)
اما القاعدة : فهي مادة قادرة على استقبال البروتون ((H+ اثناء التفاعل (مستقبل).
فمثلاً عند اذابة كلوريد الهيدروجين HCl في الماء فأنه يمنح البروتون C ويمثل الحمض، بينما يستقبل الماء البروتون H+ ويمثل القاعدة ،والمعادلة الاتية توضح ذلك :
وبهذا يمكن النظر الى التفاعلات التي يحدث فيها انتقال للبروتون على انها تفاعلات حمض وقاعدة .
- الأزواج المترافقة :
- القاعدة المرافقة : هي المادة الناتجة من منح الحمض للبروتون .
- الحمض المرافق: هي المادة الناتجة عن استقبال القاعدة للبروتون .
وبهذا يكون لكل قاعدة في التفاعل حمض مرافق في المواد الناتجة ، ويسمى الحمض وقاعدته المرافقة ، او القاعدة وحمضها المرافق ، زوجاً مترافق .
- مثال :

-
فيتضح من التفاعل يحتوي على زوجين مترافقين ، هما : الحمض وقاعدته المرافقة (HF\F-) ، والقاعدة وحمضها المرافق (H2O\H3O+) .
- مثال : حدد الأزواج المترافقة في التفاعل الاتي :
الحل
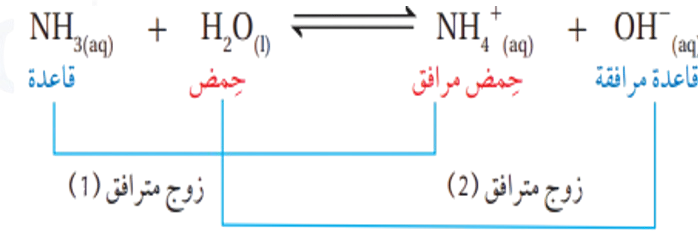
يتضح ان التفاعل يحتوي على زوجين مترافقين هما :
الحمض وقاعدته المرافقة (H2O\ OH-) .
والقاعدة وحمضها المرافق : (NH3\NH4+) .
- قوة الحمض والقاعدة :
درسنا سابقا الحموض وعرفنا انهيتأين كلياً في المحلول ، ويتجه التفاعل نحو تكوين المواد الناتجة ومثال على ذلك تفاعل الحمض :
فيتضح من المعادلة ان HCl في المحلول يسلك سلوك الحمض ، بينما يسلك الماء H2O سلوك القاعدة ؛ فأذا افترضنا حدوث تفاعل عكس فان الايون Cl- يسلك كقاعدة ، بينما يسلك H3O+ سلوك الحمض . وبما ان التفاعل يتجه كلياً نحو تكوين المواد الناتجة ؛ فان ذلك يشير الا ان الحمض HCl اكثر قدرة على منح البروتون H+ من الحمضH3O+ ، كما يشير الى ان القاعدة Cl- اقل قدرة على استقبال البروتون من القاعدة H2O وبذلك يكون H2O قاعدة اقوى من Cl- في التفاعل ؛ وبهذا نجد ان الحمض والقاعدة في جهة المواد المتفاعلة اقوى من جهة المواد الناتجة وان التفاعل يتجه نحو تكوين المواد الناتجة ، فيشير ذلك الى عدم حدوث تفاعل عكسي ؛ ولذلك يعبر عن التفاعل بسهم واحد .
اما الحموض الضعيفة فتتاين جزئيا في المحلول ، ويكون التفاعل منعكسا ، فمثلا يتاين حمض الايثانوين CH3COOH في الماء بدرجة ضئيلة كما في المعادلة التالية:
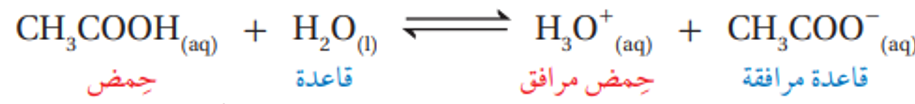
تشير درجة التأين الضئيلة للحمض CH3COOH إلى أن تركيزه في المحلول يكون عاليا مقارنة بتركيز الحمض H3O+، فيعني ذلك أن الحمض CH3COOH أقل قدرة على منح البروتون من الحمض H3O+ ؛ وبهذا يكون الحمض CH3COOH أضعف من الحمض H3O+ ، كما نجد أن القاعدة CH3COO- أكثر قدرة على استقبال البروتون من القاعدة H2O في المحلول؛ وبهذا تكون القاعدة :
CH3COO- أقوى من القاعدة H2O
وهذا يُفَسِّر حدوث التفاعل العكسي. يَتَّضِح مما سبق أن الحمض القوي HCI تكون قاعدته المرافقة CI- ضعيفة نسبيا، وأن الحمض الضعيف CH3COOH تكون قاعدته المرافقة CH3COO- قوية نسبيا، وكلما زادت قوة الحمض قلت قوة القاعدة المرافقة الناتجة عنه،وأن التفاعل يتجه نحو تكوين المواد الأضعف؛ أي أن موضع الاتزان يُزاح جهة المواد الأضعف في التفاعل. وينطبق ذلك على القواعد الضعيفة وحموضها المرافقة فالقاعدة الأقوى يكون حمضها المرافق أضعف، وكلما زادت قوة القاعدة قلت قوة الحمض المرافق الناتج عنها.
- المواد الأمفوتيرية:
يتأثر سلوك المادة كحمض أو قاعدة وفق مفهوم برونستد - لوري؛ تبعا لطبيعة المواد التي تتفاعل معها وقدرتها على منح البروتون أو استقباله، فبعض المواد تسلك كحمض في تفاعل وتسلك كقاعدة في تفاعل آخَرَ ، وتسمى مواد أمفوتيرية أو مترددة ، فمثلاً الماء في التفاعلات السابقة يسلك كقاعدة في تفاعله مع الحموض مثل حمض الهيدروكلوريك HCl ، ويسلك كحمض في تفاعله مع القواعد ، مثل تفاعله مع الامونيا NH3 ؛ وبهذا يعد الماء مادة امفوتيرية.
- مفهوم لويس :
حمض لويس : مادة يمكنها استقبال زوج او اكثر من الالكترونات اثناء التفاعل.
قاعدة لويس : مادة يمكنها منح زوج من الالكترونات اثناء التفاعل.
فمثلاً:
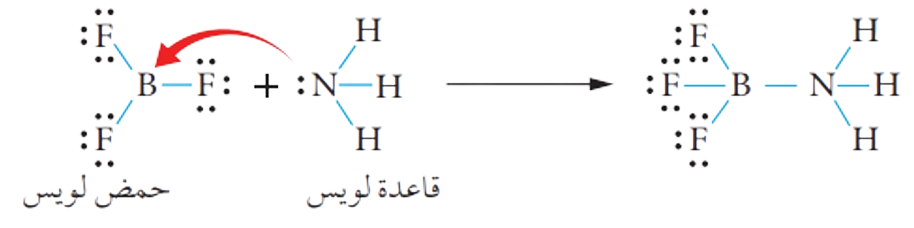
فذرة النيتروجين N تمتلك زوج إلكترونات غير رابط في NH3 يمكنها منحه؛ وبهذا فإنَّ NH3 تمثل القاعدة، في حين أن لدى ذرة البورون B في BF3 فلكا فارغا يُمَكِّنها من استقبال زوج من الإلكترونات؛ وبهذا فإن BF3 يمثل الحمض.