مُراجعة الدرس
1. الفكرةُ الرئيسةُ: أُفَسِّرُ: يأخذُ السائلُ شكلَ الإناء الذي يوضعُ فيه، ولكنّ حجمَهُ يظلُّ ثابتًا.
2. أوضِّحُ المقصود بكل ممّا يأتي:
• الضغط البخاريّ.
• درجة الغليان المعيارية.
3. أُفَسِّرُ: يغلي الماءُ في الأغوار على درجة حرارة أكثرَ قليلًا من .
4. أصِفُ: سائلٌ في وعاء مغلق ضغطُهُ البخاريّ ثابت، ما العلاقةُ بين سرعة تبخّره وسرعة تكاثف بخاره؟
5. أستنتجُ: يتبخَّر المركّبُ A بسرعة أكبرَ من سرعة تبخُّر المركّب B عند :
أ . أيُّ المركّبين قوى التجاذب بين جُزيئاته أكبر؟
ب. أيُّ المركّبين له ضغطٌ بخاريٌّ أعلى عند °25؟
جـ. أيُّ المركّبين درجةُ غليانه المعيارية أكبر؟
6. يمثّلُ المنحنى المجاورُ تغيُّر الضغط البخاريّ (mmHg) لثلاثة سوائل هي الهكسان C6H14، رابع كلوريد الكربون CCL4، وحمض الإيثانويك CH3COOH معَ درجة الحرارة C°. أجيبُ عمّا یأتي:
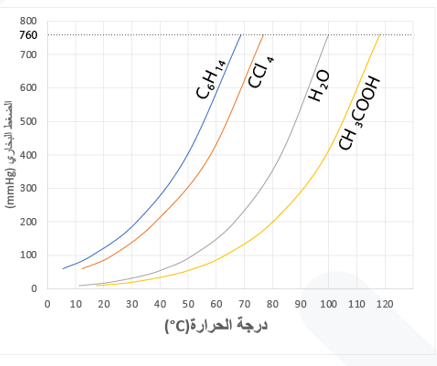
أ. أُحَدِّدُ الضغطَ البخاريَّ لرابع كلوريد الكربون عند .
ب. أُحَدِّدُ درجةَ الغليان المعيارية للهكسان.
جـ. أُرَتِّبُ السوائلَ الثلاثة حَسَبَ سرعة تبخُّرها.
د. بفرض أنّ الضغطَ الجويَّ على قمّة أحد الجبال يساوي 500mmHg، أُحَدِّدُ درجةَ غليان CCL4 عند هذا الارتفاع.
ه . أستنتجُ السائل الذي له أعلى طاقةِ تكاثف موليّة.
7. أختارُ الإجابة الصحيحة لكلّ فقرة من الفقرات الآتية:
1. المادة الأسرع تبخرا من المواد الآتية في الحالة السائلة عند الظروف نفسها:
أ. NH3 ب. H2O ج. C2H6 د. CH4
2. المركبات الآتية متقاربة في الكتلة المولية، أي منها له أعلى درجة غليان معيارية:
أ. CH3CH2OH ب. CH3CHO ج. CH3CH2F د. CH3CH2CH3
3 . يمثل المنحنى توزيع الطاقة الحركية على الجزيئات لثلاث سوائل مختلفة أعطيت الرموز الافتراضية A, B, C عند درجة حرارة معينة T، وتمثل الخطوط في الشكل الحد الأدنى من الطاقة اللازمة للتغلب على قوى التجاذب بين جزيئات كل سائل. فإن العبارة الصحيحة من العبارات الآتية هي:
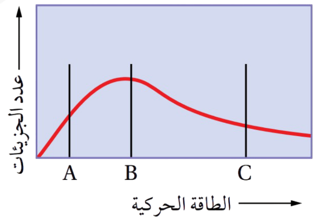
أ . درجة غليان السائل A أكبر من درجة غليان السائل .B
ب. قوى التجاذب بين جزيئات A هي الأضعف..
ج. السائل C له أقل طاقة تبخر مولية.
د . الضغط البخاري للسائل C أعلى منه للسائل
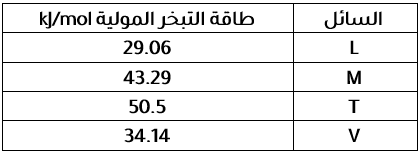
4. يتضمن الجدول الآتي قيم طاقة التبخر المولية لأربعة سوائل مختلفة أعطيت الرموز الافتراضية L, M, T, V ؛ أيٌّ منها يتوقع أن تكون قوى الترابط بين جزيئاته الأقوى؟
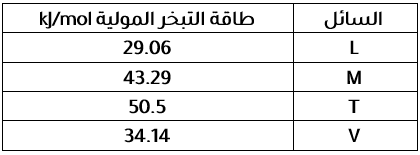
أ L ب. M ج. T د. V
إجابات أسئلة مراجعة الدرس:
السؤال الأول:
الفكرة الرئيسة: أفسر: يأخذ السائل شكل الإناء الذي يوضع فيه، ولكن حجمه يظل ثابتاً.
لأن جزيئات السائل في حركة مستمرة وعشوائية، مما يمنحه القدرة على الجريان أو الانسياب، وتأخذ شكل الإناء الذي يوضع فيه، ولأن جزيئات السائل ترتبط بقوى تجاذب ضعيفة نسبيًا تُبقيها متقاربة، فيكون له حجم ثابت.
السؤال الثاني:
أوضح المقصود بكل مما يأتي:
- الضغط البخاري: هو الضغط الناجم عن جزيئات بخار السائل والمؤثر في سطحه عند الاتزان عند درجة حرارة معينة.
- درجة الغليان المعيارية: هي درجة الحرارة التي يصبح عندها الضغط البخاري للسائل مساوياً للضغط الجوي(1 atm, 760 mmHg).
السؤال الثالث:
أفسر: يغلي الماء في الأغوار على درجة حرارة أكثر قليلاً من 100 ºC.
يغلي السائل عندما يتساوى ضغطه البخاري مع الضغط الجوي. وبما أن الضغط الجوي في منطقة الأغوار أعلى من (1 atm, 760 mmHg).وذلك بسبب انخفاضها عن مستوى سطح البحر، فلا بد أن ترتفع درجة حرارة الماء إلى أكثر من 100 ºC.
السؤال الرابع:
أصف: سائل في وعاء مغلق ضغطه البخاري ثابت، ما العلاقة بين سرعة تبخره وسرعة تكاثف بخاره؟
سرعة التبخر = سرعة تكاثف بخاره
السؤال الخامس:
أستنتج: يتبخر المركب A بسرعة أكبر من سرعة تبخر المركب B عند 25 ºC :
أ- أي المركبين قوى التجاذب بين جزيئاته أكبر؟
المركب B)) قوى التجاذب بين جزيئاته أكبر ، وذلك لأن كلما زادت قوى التجاذب بين الجزيئات، قلت سرعة التبخر
ب- أي المركبين له ضغط بخاري أعلى عند 25 ºC؟
المركب (A) له ضغط بخاري أعلى، وذلك لأن كلما كانت قوى التجاذب بين جزيئات السائل أقوى قل ضغطه البخاري والعكس.
ج- أي المركبين درجة غليانه المعيارية أكبر؟
المركب B)) درجة غليانه المعيارية أعلى، وذلك لأن درجة الغليان تعتمد على قوى التجاذب بين جزيئات السائل وتزداد بزيادتها.
السؤال السادس:
يمثل المنحنى المجاور تغير الضغط البخاري (mmHg) لأربعة سوائل مع درجة الحرارة ºC. أجيب عما يأتي:
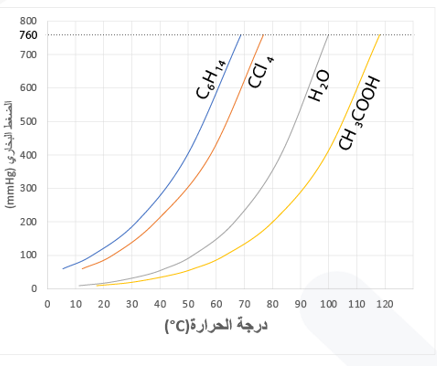
أ- أحدد الضغط البخاري لرابع كلوريد الكربون عند 60 ºC.
430mmHg تقريباً
ب- أحدد درجة الغليان المعيارية للهكسان.
68 ºC
ج- أرتب السوائل الأربعة حسب سرعة تبخرها بناءا على قوى التجاذب.
CH3COOH < H2O < CCl4 < C6H14
د- بفرض أن الضغط الجوي على قمة أحد الجبال يساوي 500mmHg، أحدد درجة غليان الماء عند هذا الارتفاع.
87 ºC
هـ- أستنتج اسم السائل الذي له أعلى طاقة تكاثف مولية.
CH3COOH، له أعلى طاقة تكاثف مولية
السؤال السابع: أختار الإجابة الصحيحة لكل فقرة من الفقرات الآتية:
1- المادة الأسرع تكاثفاً من المواد الآتية عند الظروف نفسها:
2- المركبات الآتية متقاربة في الكتلة المولية، أي منها له أعلى درجة غليان معيارية:
3 - يمثل ال لثلاث سوائل مختلفة أعطيت الرموز الافتراضية A, B, C عند درجة حرارة معينة T ، وتمثل الخطوط في الشكل الحد الأدنى من الطاقة اللازمة للتغلب على قوى التجاذب بين جزيئات كل سائل. فإن العبارة الصحيحة من العبارات الآتية هي: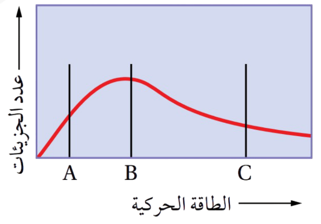
أ- درجة غليان السائل A أكبر من درجة غليان السائل B.
ب- يتوقع أن تتواجد معظم جزيئات السائل A في الحالة الغازية.
د - الضغط البخاري للسائل C أعلى منه للسائل B.
4- يتضمن الجدول الآتي قيم طاقة التبخر المولية لأربعة سوائل مختلفة أعطيت الرموز الافتراضية L, M, T, V؛ أي منها يتوقع أن تكون قوى الترابط بين جزيئاته الأقوى ؟
أ- L ب- M