1. الفكرةُ الرئيسةُ: كيفَ تتكوّنُ الروابطُ الكيميائيةُ بينَ ذراتِ العناصرِ؟
الجواب: تنشأ الروابطُ الكيميائية بين الذرات من خلال فقد الإلكترونات ، أو كسبها، أو التشارك فيها.
2- استخدم الجدولَ الدوريَّ، وأحدّدُ نوعَ الرابطةِ بينَ ذرّةِ ليثيوم وذرّةِ فلور .
الجواب: باستخدام الجدول الدوري أجدُ أن العدد الذري لليثيوم يساوي 3 ، وبذلك فإن التوزيعُ الإلكتروني لذرة
الليثيوم هو(Li: 2,1)؛ ألاحظُ من التوزيع الإلكتروني أن هذه الذرة تميلُ إلى فقد إلكترون واحد من مستوى الطاقة
الخارجي حتى تصل إلى حالة الاستقرار ، وتكون أيون الليثيوم الموجب ( +Li ).
والعدد الذري للفلور يساوي 9، وبذلك فإن التوزيعُ الإلكتروني لذرة الفلور هو (F: 2,7) ؛ ألاحظُ من التوزيع
الإلكتروني أنها تميلُ إلى كسب إلكترون واحد حتى تصل إلى حالة الاستقرار، وتكون أيون الفلوريد السالب ( -F)
وتنشأ بين الأيونين الموجب والسالب قوة تجاذب تُسمى الرابطة الأيونية .
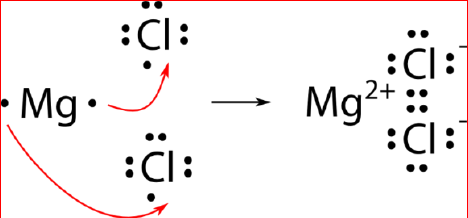
3- أوضح باستخدامِ رموزِ لويسَ كيفَ تنشأ الرابطةُ الأيونيةُ بينَ المغنيسيومِ والكلورِ.
الجواب:
4. أفسر: توصِلُ محاليلُ المركّباتِ الأيونيةِ التيارَ الكهربائيَّ.
الجواب: توصلُ محاليلُ المركبات الأيونية التيار الكهربائي لاحتوائها على الأيونات الموجبة والسالبة.
5- أقارنُ بينَ المركّباتِ الأيونيةِ والتساهميةِ من حيثُ: درجةُ الغليانِ والانصهارِ، والتوصيلُ الكهربائيُّ.

6- أطرحُ سؤالًا إجابتُهُ قوةُ الرابطةِ الأيونيةِ. .
الجواب: فسر ارتفاع درجات غليان وانصهار المركبات الأيونية؟
7. أستنتجُ: ما أنواع الروابطِ التي تنشأ بينَ كلّ منَ الذراتِ الآتيةِ :(ا لصوديومِ والكبريتِ) ،(الفلورِ والفلورِ).
الجواب: نوع الرابطة بين (الصوديومِ والكبريتِ) هي رابطة أيونية، ونوع الرابطة بين(الفلورِ والفلورِ) هي رابطة تساهمية
8. يتكوّنُ جزيءُ HCl منَ ارتباطِ ذرةِ هيدروجين بذرةِ كلور، أبيّنُ بالرسمِ هذا الترابطَ .
الجواب:
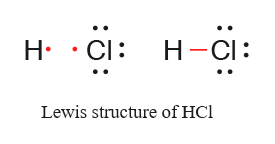
9. أكتبُ الصيغةَ الكيميائيةَ للمركّباتِ الآتيةِ: نتراتِ الصوديومِ، كبريتاتِ المغنيسيومِ.
الجواب:
نتراتِ الصوديومِ NaNO3 ، كبريتاتِ المغنيسيومِ MgSO4
10. التفكيرُ الناقدُ : يحتوي السليكون أربعة إلكترونات في مستوى التكافؤِ ، فما الرابطةُ التي يكوّنُها السليكون معَ الذراتِ الأخرى؟ أوضّحُ إجابتي .
الجواب:
بما أن السيليكون يحتوي على أربع الكترونات في مستوى التكافؤ فإنه يميل لأن يتشارك مع أربع الكترونات من ذرات أخرى، وبذلك تتكون الرابطة التساهمية.